العلاج الكيميائي لسرطان القولون والمستقيم. العلاج الكيميائي. مخاوفي - ما الذي تحقق وما لم يتحقق
في نظام علاجي قياسي مصمم لإطالة عمر المرضى الذين يعانون من أمراض الأورام في الجهاز الهضمي، إلزامييشمل العلاج الكيميائي. ويستخدم هذا على نطاق واسع في القضاء الأورام الخبيثةالطريقة تتمثل في تنفيذ استخدام قوية الأدويةمحدد التدابير العلاجية.
يجب وصف العلاج الكيميائي الإلزامي لهذا المرض لكل مريض على حدة بشكل صارم، اعتمادًا على الحالة العامة للشخص ووجود مؤشرات سريرية معينة، وشكل ومرحلة علم الأمراض التي تم تحديدها. يساعد النظام المختار بشكل صحيح ودورة العلاج المضاد للأورام على تحسين نوعية حياة مريض السرطان.
تقليديا، لسنوات عديدة، تم استخدام نوعين من الكيمياء:
العلاج الكيميائي الأحادي. هذه الطريقةهو تنفيذ دورة العلاجباستخدام دواء واحد مضاد للسرطان وغالباً ما يستخدم على دواء واحد رئيسي الجهاز الهضمي;
العلاج الكيميائي. يتضمن استخدام هذه التقنية وصف العديد من الأدوية الفعالة للمريض، والتي يجب عليه تناولها بشكل متسلسل أو متزامن.
النوع الأخير من العلاج، والذي يستخدم مجموعات معقدة إلى حد ما من العديد من الأدوية المضادة للسرطان، هو الأكثر استخدامًا. ميزتها تكمن في إمكانية تحقيق الحد الأقصى تأثير علاجيوالتي تنطوي على قمع النشاط الحيوي للخلايا المتحولة أو موتها الكامل.
في كثير من الأحيان في السنوات الاخيرةبدأ العلاج الكيميائي ليشمل العلاج الهرموني والمناعي المستهدف. إنها طرق فعالة للغاية وأقل صدمة للجسم لوقف طفرة الخلايا. أنواع هذا العلاج ومزاياها الرئيسية:
- العلاج الموجه.يوقف تكاثر ونمو الخلايا غير الطبيعية بسبب التأثيرات المستهدفة على الحمض النووي والمستقبلات ورم سرطاني.
- العلاج المناعي.يوقف تطور الخلايا الخبيثة بسبب زيادة قدرتها بمساعدة بعض الأدوية الجهاز المناعيتحديد وتدمير العملاء الأجانب.
- العلاج بالهرمونات.يزيل الأورام التي تعتمد على الهرمونات والتي لا يمكن تدميرها بالكيمياء التقليدية من خلال استخدام أدوية هرمونية خاصة.
يتم استخدام هذه الأنواع من التدابير العلاجية باستخدام أدوية العلاج الكيميائي القوية في العصر الحديث الممارسة السريريةبدأ تحديدها كأنواع مستقلة من العلاج المضاد للسرطان. يرجع تطورها السريع إلى الكفاءة العالية والحد الأدنى من موانع الاستعمال والآثار الجانبية.
ملامح الكيمياء في مراحل مختلفة من التطور
في بروتوكولات مجمع مضاد الأورام مع الأورام السرطانيةفي المعدة التي تكون في المراحل 1-2 من النمو، يتم تضمين الكيمياء كمقرر مساعد، ويمكن وصفها كما في فترة ما قبل الجراحة، وأثناء ذلك مباشرة تدخل جراحيأو بعده. في هذه المراحل من التطور الحالة المرضيةالجهاز الهضمي الرئيسي، يتم استخدام التأثير العلاجي المعقد للعديد من العوامل الصيدلانية المضادة للأورام آلية مختلفةتأثير. ترجع فعالية العلاج الكيميائي إلى حقيقة أن مكونات الدواء الفعالة، التي يتم إعطاؤها عن طريق التسريب بالتنقيط ويتم تناولها عن طريق الفم، تنتشر في جميع أنحاء الجسم بشكل جيد للغاية.
في المراحل الأخيرة من تطور العضو الهضمي الرئيسي للورم السرطاني، تزداد أهمية الكيمياء. في أغلب الأحيان، يوصف لمرضى السرطان علاجًا جهازيًا، على الرغم من أنه يوصى أحيانًا بإعطاء الأدوية المثبطة للخلايا داخل الصفاق. يتم إجراؤها من خلال شق صغير يتم إجراؤه جدار البطن. يتضمن العلاج الكيميائي للمرحلة الرابعة من سرطان المعدة مع النقائل اختيار أنواع من تدابير العلاج مثل المواد المساعدة، التي توصف بعد خضوع المريض لعملية جراحية في الجهاز الهضمي الرئيسي أو التعرض للإشعاع، والمواد المساعدة الجديدة، التي تم إجراؤها مسبقًا.
العلاج الكيميائي لسرطان المعدة في مرحلة لاحقة 3 له الأنواع التالية:
- علاجي أو علاجي، بما في ذلك العلاج المساعد والعلاج الجديد. يتم استخدامه في الحالات التي يجوز فيها التدخل الجراحي؛
- مسكنة. يهدف إلى وقف نمو الأورام غير صالحة للعمل.
في المراحل المتأخرة من السرطان، غالبا ما يوصف العلاج المضاد للورم المستقل. تنشأ الحاجة إليه فقط عندما يكون استئصال الورم أو إزالته باستخدام الإشعاع مستحيلاً. تُستخدم هذه الأنواع من العلاج الكيميائي لسرطان المعدة حصريًا في المستشفى، تحت الإشراف المباشر للطبيب. يتم وصفها أيضًا عندما لا يكون هناك تأثير للطرق الأخرى.
العلاج الكيميائي المساعد لسرطان المعدة
يعد هذا النوع من العلاج المضاد للأورام ضروريًا بعد إجراء العلاج على الجهاز الهضمي المصاب. جراحة جذرية. ولكن تجدر الإشارة إلى أن هذا العلاج الكيميائي بعد إزالة المعدة لا يجوز إلا إذا لم يكن لدى المريض علامات سريرية ونسيجية وإشعاعية لظاهرة مرضية متبقية. هدفها الرئيسي هو القضاء على النقائل المجهرية.
العلاج الكيميائي المساعد له طبيعة وقائية، لأنه يمكن أن يؤثر على الأجزاء الفردية المتبقية بعد الجراحة. خلايا غير طبيعية، المنتشرة عبر مجرى الدم. هذه الطريقة ليست علاجًا قياسيًا مضادًا للأورام وتستخدم بشكل أساسي كعلاج كيميائي وقائي بعد الجراحة. السبب الرئيسي لذلك هذا النوع الأنشطة العلاجيةولا يستخدم في جميع الحالات، هو عدم وجود أدوات متخصصة لذلك علاج فعالأورام المعدة.
بعد الجراحة، يتم أيضًا استخدام العلاج الكيميائي داخل الصفاق. تُستخدم هذه الطريقة في العلاج فقط عندما تظهر على مريض السرطان علامات تشير إلى انتشار الخلايا المتحولة من الجهاز الهضمي الرئيسي إلى السطح الداخلي للبطن. وهذا يؤدي إلى تطور الاستسقاء (تراكم السوائل في البطن). أثناء دورة العلاج الكيميائي، يقوم المتخصصون بإزالتها باستخدام القسطرة. ومن خلاله، يتم سكب أدوية العلاج الكيميائي المذابة والمسخنة إلى 40 درجة مئوية في الصفاق. بالإضافة إلى ذلك، باستخدام الكيمياء داخل الصفاق لإزالة الأدوية من الجسم، يتم وصف السوائل الوريدية ومضادات القيء لمرضى السرطان.
العلاج الكيميائي المساعد الجديد لسرطان المعدة
يتم تنفيذ طريقة العلاج هذه، على عكس العلاج المساعد، مباشرة قبل بدء المسار الرئيسي للعلاج. هدفها الرئيسي هو تقليل حجم الورم الرئيسي لتسهيل الجراحة وبالتالي تحسين نتائجها.
يتكون العلاج الكيميائي المساعد الجديد القياسي لسرطان المعدة من استخدام نظام التيار المتناوب الأمثل:
- أدرياميسين، وهو نظير شائع الاستخدام وهو دوكسوروبيسين. يوصف الدواء عن طريق الوريد بجرعة 45 ملغم / متر مربع في اليوم.
- سيكلوفوسفاميد. يتم أيضًا إجراء العلاج الكيميائي قبل الجراحة لإزالة سرطان المعدة باستخدام هذا الدواء باستخدام الحقن في الوريد. الجرعة المقبولة عمومًا هي 500 ملجم/متر مربع يوميًا.
يتضمن العلاج الكيميائي قبل الجراحة وفقًا لنظام AC تكراره ست مرات بفاصل 3 أسابيع. يهتم العديد من المرضى بمسألة كيفية حساب مساحة الجسم. يتم ذلك عادة من قبل الأطباء عند وصف الدواء، ولكن ل معلومات عامةيجب أن يقال أنه يتم استخدام صيغة Mosteller لهذا الغرض. ومعنى ذلك أنه من الضروري استنتاج الجذر التربيعي لوزن الجسم بالكيلو جرام مضروبًا في الطول بالسنتيمتر ومقسمًا على 3600.
العلاج الكيميائي الملطف
يجب أن تكون التغذية أثناء العلاج الكيميائي لسرطان المعدة محدودة، لأن مرضى السرطان لا يستطيعون تحمل العديد من الأطعمة المألوفة. ينطبق هذا بشكل أساسي على الأطعمة الدهنية والثقيلة والأطباق الساخنة وكذلك المخللات والتوابل الحارة. من غير المقبول أيضًا شرب الكحول، لأن المشروبات الكحولية يمكن أن تؤدي بسهولة إلى الانتكاس.
التغذية بعد العلاج الكيميائي تتطلب الالتزام بها قواعد معينةوجبات:
- يجب أن يحتوي الجزء الأكبر من المنتجات الموجودة على طاولة الشخص المريض على كمية متزايدة من المعادن و مجمعات الفيتاميناتوكذلك البروتين؛
- من الضروري الحفاظ على نظام غذائي كسري، أي تناول الطعام في كثير من الأحيان، ولكن في أجزاء ضئيلة؛
- يجب استبعاد جميع الأطباق التي تحتوي على أطعمة مزعجة من النظام الغذائي اليومي.
يجب أن يلبي النظام الغذائي للعلاج الكيميائي لسرطان المعدة الموصوف في فترة ما بعد الجراحة متطلبات معينة بشكل مباشر. يتم إعطاء الأهمية الأساسية في هذه الحالة لاستهلاك المنتجات المهمة لعمل الجسم، والتي تحتوي على الحد الأدنى من الدهون وأي عناصر كيميائية دقيقة يمكن أن يكون لها تأثير مزعج على الغشاء المخاطي للجهاز الهضمي.
تعتبر مراقبة توافق المنتج أمرًا مهمًا أيضًا. فقط عندما تكون مناسبة بشكل مثالي لبعضها البعض، فإن خطر حدوث أضرار إضافية في المعدة، والتي يمكن أن تؤدي إلى انتكاسة المرض، مصحوبة بزيادة ألم. بشكل منفصل، ينبغي أن يقال عن تغذية مرضى السرطان في المرحلة الأخيرة المتقدمة من السرطان. ومن أجل الحفاظ على الوظائف الحيوية لأجسامهم، يتم إعطاؤهم عن طريق الوريد من خلال قطارة ومحلول ملحي وبروتينات وجلوكوز.
كيفية استعادة المعدة بعد العلاج الكيميائي؟
على الرغم من الفعالية العالية للعلاج الكيميائي، إلا أنه مطلوب بعد مساره معاملة خاصةواستعادة عمل الأعضاء المتضررة أثناء التدابير العلاجية. المهام الرئيسية في هذه الحالة هي تطبيع الأداء الأنظمة الداخليةالجسم، وتقوية جهاز المناعة لدى الإنسان، وتخليصه من التسمم، أي القضاء على الاضطرابات الناجمة عن تناول الأدوية القوية.
يحتاج كل مريض محدد إلى برنامج فردي لاستعادة الجسم، والذي لا يشمل النظام الغذائي فحسب، بل أيضًا علاج بدنيوالسباحة والتصريف اللمفاوي والعلاج بالرائحة والعصير وتطهير الجسم باستخدام مغلي الأعشاب.
تتضمن استعادة المعدة بعد العلاج الكيميائي المرور بمراحل إعادة تأهيل معينة:
- القضاء على المشتركة التسمم الشديد. نتائج جيدةيتم تحقيقها من خلال تعزيز نظام الشربمغلي التوت و اعشاب طبيةوكذلك المدخول المنتظم من المركبات النباتية المدرة للبول.
- إزالة المواد السامة من الجهاز الهضمي. لهذا، يتم استخدام النباتات المفرزة للمخاط، على سبيل المثال بذور الكتان، الخطمي أو حشيشة الملاك، بوليفيبان والكربون المنشط؛
- تصحيح دسباقتريوز. للقيام بذلك، استخدم تركيبة محضرة على أساس مزيج من الأعشاب مثل السيتراريا الأيسلندية والزعتر الزاحف وإكليل الجبل البري؛
- تتم استعادة البكتيريا الدقيقة في الجهاز الهضمي باستخدام سلالات حية البكتيريا النافعة، والتي في كميات كبيرةوجدت في بعض منتجات حمض اللاكتيك.
مطلوب برنامج شفاء للقضاء على الأورام الخبيثة من الجهاز الهضمي حتى عندما يتم اختيار العلاج الكيميائي لسرطان المعدة بشكل صحيح من قبل أخصائي ويتضمن فقط الأدوية الحديثة عالية الفعالية التي تمنع حدوث معظم الآثار الجانبية المحتملة.
غالبًا ما يهتم المرضى بكيفية عمل العلاج الكيميائي لسرطان المعدة؟ إن معرفة إجابة هذا السؤال تسمح للشخص المصاب بالسرطان بالاستعداد لجميع الفروق الدقيقة في طريقة العلاج هذه. وفقا لكبار الخبراء، تستخدم لذلك الأدويةلا يمكن أن تستلزم فقط عدد كبير من عواقب سلبيةولكنها تؤدي إلى تدهور كبير في الحالة العامةمريض.
هذا هو السبب في أن الأطباء المعالجين يزنون بعناية جميع الإيجابيات والسلبيات قبل وصف دورة معينة. أيضًا، أثناء هذا العلاج، يقوم أطباء الأورام بإجراء فحوصات منتظمة لمراقبة فعاليته. الفحوصات التشخيصية. إنها تجعل من الممكن إجراء التعديلات اللازمة على المسار العلاجي.
فيديو إعلامي:
مركز أبحاث الأورام الروسي سمي بهذا الاسم. ن.ن. رامز بلوخين، موسكو
العلاج الكيميائي لسرطان المعدة.
S. A. تيلاندين
نجاح العلاج الكيميائي لسرطان المعدة متواضع. هناك حاجة واضحة للبحث عن أدوية جديدة فعالة مضادة للأورام ومجموعاتها.
ستنظر هذه الورقة في دور العلاج الدوائي لدى مرضى سرطان المعدة، وعلى وجه الخصوص، أهمية العلاج الكيميائي في علاج المرضى المنتشرين والعلاج قبل الجراحة في المرضى الذين يعانون من مرض متقدم محليًا، بالإضافة إلى إمكانية العلاج الكيميائي المساعد للمعدة القابلة للجراحة. سرطان.
سرطان المعدة المنتشر
هل العلاج الكيميائي ضروري لمرضى سرطان المعدة النقيلي؟
قد يبدو هذا السؤال غير مناسب للبعض، ولكن في عيادتنا غالبًا ما نلتقي بمرضى نصحوا برفض العلاج الكيميائي. يُظهر الجراحون العاملون في مستشفيات الجراحة العامة شكوكًا خاصة فيما يتعلق بإمكانيات العلاج الكيميائي. أساس هذه الشكوك هو عدم قدرة العلاج الكيميائي الحديث على علاج مرضى سرطان المعدة. ومع ذلك، فقد أثبتت التجارب العشوائية التي تقارن نتائج العلاج الكيميائي وعلاج الأعراض بشكل مقنع حقيقة ذلك علاج بالعقاقيريزيد متوسط العمر المتوقع لدى المرضى الذين يعانون من عملية النقيلي من 3-5 أشهر إلى 10-12 شهرًا (الجدول 1). وبناءً على نتائج هذه الدراسات، أصبح من غير الأخلاقي رفض العلاج الكيميائي لمريض مصاب بسرطان المعدة المنتشر.
الجدول 1. مقارنة فعالية العلاج الكيميائي وعلاج الأعراض في المرضى الذين يعانون من سرطان المعدة النقيلي
|
عدد المرضى |
عمر |
|
|
فامتكس |
10 أشهر |
|
|
علاج الأعراض |
3 اشهر |
|
|
FBMTX |
12 شهر |
|
|
علاج الأعراض |
3 اشهر |
|
|
قزم |
10 أشهر |
|
|
علاج الأعراض |
4 اشهر |
|
|
قزم |
10.2 أشهر |
|
|
علاج الأعراض |
5 شهور |
فعالية الأدوية المضادة للأورام المختلفة في سرطان المعدة
في الجدول يوضح الجدول 2 تواتر التأثيرات الموضوعية عند وصف الأدوية المضادة للأورام المختلفة في المرضى الذين يعانون من سرطان المعدة النقيلي. فعاليتها لا تتجاوز 30%، مما يدل على انخفاض حساسية مرضى سرطان المعدة للأدوية المتوفرة لدينا. حتى وقت قريب، كان الدواء الرئيسي لعلاج سرطان المعدة هو 5-فلورويوراسيل. في الوقت الحاضر، يكتسب سيسبلاتين، وتاكسان، وإرينوتيكان شعبية متزايدة.
ما هو أكثر فعالية: 5 فلورويوراسيل أم توليفات؟
لا يوجد حتى الآن دليل مقنع على أن العلاج الأحادي 5 فلورويوراسيل أقل فعالية من العلاج الكيميائي المركب مع أو بدون 5 فلورويوراسيل. لا يوجد سوى دراستين عشوائيتين في الأدبيات (الجدول 3) تقارنان فعالية 5-فلورويوراسيل والتوليفات المبنية عليه. وقد تبين أنه عند إجراء
الجدول 2. فعالية الأدوية المضادة للأورام المختلفة في المرضى الذين يعانون من سرطان المعدة المنتشر
|
المخدرات |
عدد المرضى |
التأثير الموضوعي،٪ |
|
مضادات الأيض: |
||
|
5-فلورويوراسيل |
416 |
|
|
الميثوتريكسيت |
||
|
جيمسيتابين |
||
|
UFT |
188 |
|
|
هيدروكسي يوريا (لكل نظام تشغيل) |
||
|
فتورافور (لكل نظام تشغيل) |
||
|
مضادات حيوية: |
||
|
ميتوميسين-C |
211 |
|
|
دوكسوروبيسين |
141 |
|
|
إيبيروبيسين |
||
|
مشتقات البلاتين: |
||
|
سيسبلاتين |
139 |
|
|
كاربوبلاتين |
||
|
التاكسانات: |
||
|
باكليتاكسيل |
||
|
دوسيتاكسيل |
123 |
|
|
مثبطات التوبويزوميراز: |
||
|
irinotecan |
||
|
com.topotecan |
غالبًا ما يكون للعلاج الكيميائي المركب تأثير موضوعي مضاد للأورام، والذي، مع ذلك، لا يؤدي إلى زيادة في متوسط العمر المتوقع مقارنة باستخدام العلاج الأحادي 5 فلورو يوراسيل. وينبغي الاعتراف بأن العدد القليل من المرضى المشاركين في هذه الدراسات لا يسمح لنا بالحديث عن الموثوقية الإحصائية للنتائج التي تم الحصول عليها. في الوقت نفسه، في معظم دول العالم، أدت إمكانية تحقيق تأثير أكبر مضاد للأورام إلى ترجيح كفة الميزان لصالح وصف العلاج الكيميائي المركب.
ما هو نظام العلاج الكيميائي المركب القياسي للعلاج الكيميائي في الخط الأول؟
الجواب على هذا السؤال موجود في دول مختلفةوسيكون الأمر مختلفًا في القارات المختلفة. لم تظهر أي من المجموعات التي تمت دراستها في الدراسات العشوائية مزايا مقنعة على غيرها. ببساطة، لا يوجد أي منها فعال بما يكفي لعلاج سرطان المعدة. أظهرت العديد من المجموعات المقترحة في البداية نتائج مبهرة. ومع ذلك، عند إجراء دراسات عشوائية، لم يتمكن أي منها من تأكيد النتائج التي تم الحصول عليها مسبقًا (الجدول 4).
في الثمانينيات، كانت التركيبة الأكثر شيوعًا هي FAM (5-فلورويوراسيل، ودوكسوروبيسين، وميتوميسين-C)، والتي كانت فعاليتها في الدراسات الأولى أكثر من 40٪. ومع ذلك، في التجارب العشوائية، كان متوسط العمر المتوقع مشابهًا بين FAM و5-فلورويوراسيل، وفي الدراسات الحديثة، انخفضت فعالية مجموعة FAM إلى 9-25٪. في أوائل التسعينيات، بعد تجربة عشوائية أظهرت فيها مجموعة FAM نتائج أسوأ، تم استبدالها بتركيبة FAMTX (5-فلورويوراسيل، دوكسوروبيسين، ميثوتريكسات). تم اعتبار مجموعة FAMTX معيارًا للعلاج الكيميائي لسرطان المعدة المنتشر. عند مقارنتها
الجدول 3. نتائج المقارنة بين فعالية 5-فلورويوراسيل والتوليفات المستندة إليه
المرضى الذين يعانون من سرطان المعدة النقيلي
|
عدد المرضى |
التأثير الموضوعي،٪ |
العمر المتوقع، أشهر |
|
|
5-فو |
|||
|
5-FU + دوكسوروبيسين |
|||
|
مألوف |
|||
|
5-فو |
7,5 |
||
|
مألوف |
|||
|
103 |
الجدول 4. نتائج التجارب العشوائية في المرضى الذين يعانون من سرطان المعدة النقيلي
|
مصدر أدبي |
وضع |
رقم |
موضوعي |
مدة |
|
مريض |
تأثير، ٪ |
الحياة، أشهر |
||
|
ويلس ج. وآخرون (1991) |
مألوف |
103 |
7,2 |
|
|
فامتكس |
105 |
10,5* |
||
|
كيلسن د. وآخرون. (1991) |
فامتكس |
|||
|
EAP |
||||
|
فانهوفر يو وآخرون. (2000) |
فامتكس |
6,7 |
||
|
قزم |
7,2 |
|||
|
7,2 |
||||
|
كوكوني جي وآخرون. (2001) |
فامتكس |
200 |
6,9 |
|
|
ثروة |
7,7 |
|||
|
ويب أ. وآخرون. (1997) |
فامتكس |
130 |
6,1 |
|
|
ECF |
126 |
8,7 * |
*ص<0.05.
مع مزيج من EAP (إيتوبوسيد، دوكسوروبيسين، سيسبلاتين) بنفس الفعالية، تبين أن FAMTX أقل سمية.
في أواخر التسعينيات، بدأ استخدام المجموعات التي تحتوي على البلاتين بشكل متزايد. أحد هذه الأنظمة هو تركيبة PF، والتي، بعد إعطاء سيسبلاتين، يتم توفير تسريب طويل الأمد لـ 5 فلورويوراسيل لمدة 5 أيام.
في دراسة EORTC، تقرر مقارنة فعالية مجموعات FAMTX وPF وELF (إيتوبوسيد، ليوكوفورين، 5-فلورويوراسيل). تم اقتراح ELF لعلاج كبار السن والمرضى الضعفاء باعتبارهم يعانون من حد أدنى من السمية، وهو شائع بسبب سهولة تنفيذه وإمكانية العلاج في العيادات الخارجية. وكانت النتائج مخيبة للآمال. ولم تتجاوز فعالية التركيبات الثلاث 20%، وكان متوسط العمر المتوقع هو نفسه وبلغ حوالي 7 أشهر. وخلص الباحثون إلى أنه لا يمكن اعتبار أي من المجموعات المدروسة معيارًا للعلاج الكيميائي لدى المرضى الذين يعانون من سرطان المعدة المنتشر، وشددوا على الحاجة إلى تطوير مجموعات جديدة.
كما فشلت مجموعة أخرى من PELF المحتوية على السيسبلاتين (سيسبلاتين وإبيروبيسين وليوكوفورين و5 فلورويوراسيل) في إثبات تفوقها على نظام FAMTX، وكان حدوث الآثار الجانبية أعلى في مجموعة PELF.
اليوم، تُعرف نتائج دراسة واحدة فقط، حيث أظهرت مجموعة FAMTX نتائج أكثر تواضعًا مقارنةً بتركيبة ECF المحتوية على البلاتين cis (الإيبيروبيسين، والسيسبلاتين، والحقن طويلة المدى لـ 5 فلورويوراسيل). كانت معدلات التأثير الموضوعي (46% مقابل 21%) ومتوسط البقاء على قيد الحياة (8.7 مقابل 6.1 أشهر) أفضل بكثير بالنسبة لـ ECF. وهكذا، فإن التوليفات مع إدراج سيسبلاتين تحسنت بشكل طفيف فقط من تشخيص المرضى الذين يعانون من سرطان المعدة النقيلي.
تشير البيانات المذكورة أعلاه إلى أنه لا توجد معايير للعلاج الدوائي للمرضى الذين يعانون من سرطان المعدة النقيلي. يعتبر PF هو المعيار في الولايات المتحدة الأمريكية وكوريا واليابان، في حين يتم استخدام ECF في كثير من الأحيان في أوروبا. كثيرون، مع الأخذ في الاعتبار أن التركيبات التي تحتوي على سيسبلاتين شديدة السمية، يفضلون استخدام أنظمة "خالية من البلاتين" (ELF أو FAMTX). من حيث الفعالية الفورية، تتمتع مجموعات البلاتين ببعض المزايا، والتي، مع ذلك، لا تؤثر بشكل كبير على متوسط العمر المتوقع للمرضى الذين يعانون من سرطان المعدة المنتشر.
يجب أن يتم تحديد اختيار هذا النظام أو ذاك حسب الحالة السريرية المحددة، وعلى وجه الخصوص، الحالة العامة للمريض. وبالتالي، عند علاج المرضى الصغار في حالة مرضية بشكل عام دون حدوث مضاعفات مرتبطة بها مثل النزيف، فإننا نفضل وصف أنظمة تحتوي على البلاتين، مثل MEP. في المرضى المسنين والضعفاء، التركيبة المفضلة هي ELF، والتي لها سمية معتدلة ويمكن إجراؤها في العيادات الخارجية.
كيفية تحسين نتائج العلاج الكيميائي؟
في السنوات الأخيرة، زاد الاهتمام باستخدام التاكسان والإرينوتيكان لعلاج المرضى المصابين بسرطان المعدة. في العلاج الأحادي، كانت فعالية هذه الأدوية 21-23٪. كان الجمع بين دوسيتاكسيل وسيسبلاتين فعالاً في 16 (37%) من 39 مريضاً بمتوسط عمر متوقع يبلغ 10.4 أشهر.
في دراسة أجراها E. فان Cutsem وآخرون. تم تعيين المهمة لتحديد التركيبة المثالية بما في ذلك الدوسيتاكسيل في المرضى الذين يعانون من سرطان المعدة. عند مقارنة مزيج TC (دوسيتاكسيل وسيسبلاتين) وTCF (دوسيتاكسيل وسيسبلاتين و5-فلورويوراسيل)، أظهرت كلتا التوليفتين فعالية عالية في مكافحة الأورام (كان معدل التأثير الموضوعي 35% و56%، على التوالي) وطولًا كبيرًا من الوقت للتقدم. (5.0 و 5.9 شهرًا على التوالي) مع تكرار متساوٍ للآثار الجانبية. بناءً على ذلك، تم اختيار تركيبة TCF للاختبار في تجربة عشوائية مقارنة حيث يتلقى المرضى في المجموعة الضابطة دفعات من السيسبلاتين و5 فلورويوراسيل.
قارنت دراسة تعاونية أخرى فعالية وسمية مزيج من IP (إرينوتيكان وسيسبلاتين) وIFU (إرينوتيكان وليوكوفورين و5 فلورويوراسيل) في المرضى الذين يعانون من سرطان المعدة المتقدم. كان معدل التأثيرات الموضوعية في مجموعة IP 28%، في مجموعة IFU - 39%، والذي كان بمثابة الأساس لمزيد من الدراسة لمجموعة IFU في تجربة عشوائية. وبالتالي، فمن الممكن أن تحدد نتائج التجارب العشوائية الجارية قيمة دوسيتاكسيل وإرينوتيكان في العلاج الكيميائي المركب لسرطان المعدة المنتشر.
تتم أيضًا دراسة إمكانية استخدام الفلوروبيريميدينات الجديدة عن طريق الفم (capecitabine، UFT) في العلاج الكيميائي المركب، والتي، في بارامتراتها الدوائية، تحاكي الحقن الوريدي طويل الأمد لـ 5-فلورويوراسيل. في هذا الصدد، يبدو من المنطقي استبدال الحقن المطولة لـ 5-فلورويوراسيل، والتي تعتبر مرهقة جدًا للموظفين والمرضى، بكابيسيتابين عن طريق الفم أو UFT في تركيبة ECF. لقد ثبت أن الكابيسيتابين بجرعة 1000 مجم/م2 مرتين في اليوم بالاشتراك مع سيسبلاتين بجرعة 60 مجم/م2 في اليوم الأول وإيبيروبيسين بجرعة 50 مجم/م2 كل 3 أسابيع يتمتع بقدرة تحمل مرضية وفعالة. في 39% من المرضى المصابين بسرطان المعدة. أظهر تحليل الحرائك الدوائية أن الكابيسيتابين يمتص جيدًا حتى في المرضى الذين خضعوا سابقًا لاستئصال المعدة، في حين أن تركيز الدواء في الدم يشبه تركيزه أثناء الحقن الوريدي طويل الأمد لـ 5 فلورويوراسيل.
لعلاج 50 مريضًا مصابًا بسرطان المعدة النقيلي، تم استخدام تركيبة تتضمن الإبيروبيسين 50 ملغم/م2 في اليوم الأول، والسيسبلاتين 60 ملغم/م2 في اليوم الأول وUFT 360 ملغم/م2 عن طريق الفم يوميًا لمدة 21 يومًا مع تناول متزامن عن طريق الفم لـ 50 مريضًا بسرطان المعدة النقيلي. يوكوفورين بجرعة 45 ملغ، تم تنفيذ الدورة الثانية من العلاج في اليوم الثامن والعشرين. كان تكرار التأثيرات الموضوعية للتركيبة المدروسة 54.3% مع متوسط العمر المتوقع 10 أشهر. تتمثل ميزة التركيبة المقترحة في الإدارة الملائمة للفلوروبيريميدين لكل نظام تشغيل بدلاً من دفعات 5 فلورويوراسيل في نظام ECF الكلاسيكي.
هل من الممكن إطالة التأثير المضاد للورم الذي تم تحقيقه أثناء العلاج الكيميائي لدى مرضى سرطان المعدة باستخدام مثبطات تكوين الأوعية الدموية؟ جيه فيلدنج وآخرون. أظهرت نتائج دراسة عشوائية درست فعالية دواء جديد مضاد لتولد الأوعية من مجموعة مثبطات البروتين المعدني - الماريماستات. شملت الدراسة 369 مريضاً يعانون من سرطان المعدة المنتشر مع تأثيرات موضوعية أو استقرار المرض في نهاية العلاج الكيميائي. وعندما توقف العلاج الكيميائي، تم إعطاؤهم علاجًا وهميًا أو ماريماستات. أدى تناول الماريماستات إلى زيادة كبيرة في وقت التقدم من 135 يومًا في مجموعة الدواء الوهمي إلى 167 يومًا في مجموعة الماريماستات. وكانت معدلات البقاء على قيد الحياة لمدة عام واحد 14٪ و 20٪ على التوالي.
العلاج الكيميائي الخط الثاني لسرطان المعدة
اليوم لا توجد توصيات مقبولة بشكل عام للعلاج الكيميائي من الخط الثاني في المرضى الذين يعانون من سرطان المعدة المنتشر. يمكنني فقط مشاركة تجربة قسمنا. إذا تم استخدام مجموعة تحتوي على سيسبلاتين (على سبيل المثال MEP أو PF أو TPF) كخط أول للعلاج الكيميائي، فمع تقدم العملية، يتم وصف تركيبة ELF في أغلب الأحيان. إذا تم استخدام تركيبة ELF في المرحلة الأولى، فسيتم وصف مجموعات تشمل سيسبلاتين (سيسبلاتين-ميتوميسين-C) كخط ثانٍ من العلاج الكيميائي في حالة مرضية بشكل عام. بالإضافة إلى ذلك، يمكن استخدام الفلوروبيريميدينات عن طريق الفم، مثل كابيسيتابين أو UFT أو فتورافور، في العلاج الكيميائي في الخط الثاني.
سرطان المعدة المتقدم محليا
بالنسبة لسرطان المعدة T3-4، تمثل الجراحة الجذرية تحديًا تقنيًا. وبالإضافة إلى ذلك، في هذه المرحلة من الورم الرئيسي هناك احتمال كبير لانتشار ورم خبيث إلى الغدد الليمفاوية الإقليمية. في هذا الصدد، يصبح العلاج الكيميائي المساعد الجديد مبررًا، والذي، في حالة نجاحه، يحسن إمكانية إجراء جراحة جذرية ويدمر النقائل الدقيقة البعيدة. ولسوء الحظ، لم يتم تأكيد جدوى هذا النهج بعد من خلال بيانات الدراسات ذات الصلة. في تجربتين عشوائيتين، لم يؤد العلاج الكيميائي المساعد الجديد إلى زيادة كبيرة في معدل الاستئصال الجذري، وبالتالي إلى تحسن في النتائج على المدى الطويل مقارنة بالجراحة دون علاج دوائي سابق. في هذه الدراسات، تم استخدام مجموعات من FAMTX وPF كعلاج كيميائي، والذي، كما هو موضح سابقًا، له تأثير طفيف مضاد للأورام في سرطان المعدة. إن الفعالية المنخفضة للمجموعات المستخدمة هي التي يمكن أن تفسر فشل العلاج المساعد الجديد. ونأمل أن يؤدي إدخال مجموعات جديدة بما في ذلك تاكسان وإرينوتيكان وأدوية أخرى إلى زيادة فعالية العلاج المساعد الجديد في المرضى الذين يعانون من سرطان المعدة المتقدم محليًا. ومن المهم أيضًا تحديد العوامل التي تتنبأ بفعالية العلاج الكيميائي المخطط له لدى مريض معين.
سرطان المعدة القابل للجراحة
يتم تحديد تشخيص المرضى الذين يعانون من سرطان المعدة القابل للجراحة في المقام الأول من خلال مرحلة المرض. أكثر من 80% من مرضى T1-2N0M0 يتعافون بعد الجراحة الجذرية. ينخفض معدل البقاء على قيد الحياة لمدة 5 سنوات إلى 50% في وجود T3 ولا يزيد عن 20% في وجود نقائل إلى العقد الليمفاوية الإقليمية. من هذه المواقف، ليس هناك شك في الحاجة إلى العلاج الجهازي المساعد في المرضى الذين يعانون من سرطان المعدة القابل للجراحة.
ومع ذلك، حتى الآن لا توجد بيانات مقنعة حول فوائد العلاج المساعد في المرضى الذين يعانون من سرطان المعدة القابل للجراحة. هناك تقارير معزولة في الأدبيات حول التحسن
الجدول 5. نتائج التجارب العشوائية للعلاج المساعد في المرضى الذين يعانون من سرطان المعدة القابل للجراحة.
|
مصدر أدبي |
وضع |
رقم |
مدة |
5 سنوات من العمر |
|
مريض |
الحياة، أشهر |
معدل البقاء على قيد الحياة،٪ |
||
|
ألوم دبليو وآخرون (1989) |
ميتوميسين-S-5FU |
141 |
||
|
ميتوميسين-S-5FU-CMFP |
140 |
|||
|
يتحكم |
130 |
|||
|
كومبس ر. وآخرون. (1990) |
مألوف |
133 |
||
|
يتحكم |
130 |
|||
|
ناكاجيما ت. وآخرون. (1999) |
ميتوميسين-C-UFT-araC |
288 |
||
|
يتحكم |
285 |
|||
|
هاليسي م. وآخرون. (1994) |
يتحكم |
145 |
||
|
لتر (SOD 46 غراي) |
138 |
|||
|
مألوف |
159 |
|||
|
دوكرو م. وآخرون. (2000) |
5-فو |
127 |
||
|
يتحكم |
133 |
|||
|
دي بارتولوميو م وآخرون. (2000) |
إيب-5-فو |
137 |
||
|
يتحكم |
137 |
ومع ذلك، لم تؤكد أي دراسة عشوائية كبيرة استصواب العلاج المساعد في هذه الفئة من المرضى.
أنا. بانزيني وآخرون. عرض نتائج التحليل التلوي لـ 17 تجربة عشوائية تدرس دور العلاج الكيميائي المساعد، والتي شملت ما مجموعه 2913 مريضًا يعانون من سرطان المعدة القابل للاستئصال. أدى استخدام العلاج الكيميائي مع الجراحة إلى تقليل خطر الوفاة بنسبة 14٪ مقارنة بالجراحة دون علاج كيميائي. تشير هذه النتائج إلى تحسن متواضع للغاية في البقاء على قيد الحياة في مجموعة المرضى الذين تلقوا العلاج الكيميائي المساعد.
في الجدول يوضح الجدول 5 نتائج التجارب العشوائية على العلاج المساعد لسرطان المعدة والتي شملت أكثر من 100 مريض في كل مجموعة من المجموعات المقارنة. لم يُظهر أي منهم تحسنًا في نتائج العلاج على المدى الطويل عند تناول العلاج المساعد باستخدام مجموعات تشمل الميتوميسين-C أو مشتقات البلاتين. في دراسة أجراها M. هاليسي وآخرون. تم إجراء العلاج الإشعاعي (SOD-46 Gy) كعلاج مساعد، مما أدى إلى تفاقم نتائج العلاج مقارنة بالتحكم.
الدراسة الوحيدة التي أظهرت جدوى العلاج المساعد بعد استئصال المعدة الجذري هي دراسة SWOG-Intergroup. تم اختيارهم بصورة عشوائية 603 المرضى الذين يعانون من سرطان غدي في المعدة أو تقاطع المريء والمعدة من المراحل Ib-IV بعد إجراء عملية جراحية جذرية إلى مجموعتين. في المجموعة الأولى، لم يتلق المرضى العلاج المساعد. المجموعة الثانية تلقت العلاج وفق النظام التالي:
- دورة واحدة من العلاج الكيميائي باستخدام 5-فلورويوراسيل 425 مجم/م2 وليوكوفورين 20 مجم/م2 أيام 1-5
- دورة قصيرة من العلاج الكيميائي باستخدام 5-فلورويوراسيل 400 ملغم/م2 وليوكوفورين 20 ملغم/م2 أيام 1-4 في الأسبوع الأول من العلاج الإشعاعي
- العلاج الإشعاعي الجرعة الإجمالية 45 غراي في الكسور1.8 غراي لكل منهما
- دورة قصيرة من العلاج الكيميائي باستخدام 5-فلورويوراسيل 400 ملغم/م2 وليوكوفورين 20 ملغم/م2 في الأيام 1-3 في الأسبوع الأخير من العلاج الإشعاعي
الجدول 6. نتائج العلاج الكيميائي المساعد مقارنة مع الملاحظة في المرضى الذين يعانون من سرطان المعدة بعد العلاج الجراحي
|
ملاحظة |
HT+LT |
|
|
عدد المرضى |
275 |
281 |
|
مدة الفترة الخالية من الانتكاسات |
19 شهرا |
30 شهرا |
|
عمر |
28 شهرا |
35 شهرا |
|
معدل البقاء على قيد الحياة لمدة 3 سنوات |
40% |
50% |
|
معدل البقاء على قيد الحياة لمدة 4 سنوات |
30% |
46% |
|
الانتكاسات الأولى: |
||
|
في ما تبقى من المعدة أو مفاغرة |
29% |
19% |
|
العقد الليمفاوية الإقليمية |
72% |
68% |
|
الانبثاث البعيدة |
18% |
35% |
- دورتان من العلاج الكيميائي باستخدام 5-فلورويوراسيل 425 ملغم/م2 وليوكوفورين 20 ملغم/م2 في الأيام 1-5 بعد شهر واحد.
على الرغم من أن العلاج الكيميائي كان سامًا، إلا أنه كان مقبولًا بشكل عام. تم الإبلاغ عن 3 حالات وفاة بسبب التسمم؛ لوحظت سمية من الدرجة الثالثة إلى الرابعة في 73٪ من المرضى (أمراض الدم، الجهاز الهضمي، المعدية). وترد في الجدول نتائج الدراسة بعد 4 سنوات من الملاحظة. 6.
باختصار، أظهرت هذه الدراسة تحسنًا كبيرًا بنسبة 10٪ في البقاء على قيد الحياة لمدة 3 سنوات لدى المرضى الذين يتلقون العلاج المركب المساعد، وذلك بسبب انخفاض عدد انتكاسات المرض في الجزء المتبقي من المعدة والتقدم بسبب النقائل البعيدة. ربما يصبح نظام العلاج هذا معيارًا جديدًا لعلاج مرضى سرطان المعدة المعرضين لخطر كبير للانتكاس (المرحلتين الثانية والثالثة) بعد العلاج الجراحي الجذري.
الإدارة داخل الصفاق من الأدوية المضادة للورم
لهذا الغرض، يتم استخدام سيسبلاتين بجرعة 75-100 ملغ، بليوميسين 60 ملغ، ThioTEF 40-60 ملغ. مع طريقة الإعطاء هذه، يتم إنشاء تركيز عالٍ من الأدوية المضادة للأورام في تجويف البطن لفترة طويلة. ليس هناك فائدة من إعطاء السيكلوفوسفاميد داخل الصفاق، لأن السيكلوفوسفاميد نفسه ليس له نشاط مضاد للأورام. فقط في الكبد، تحت تأثير إنزيم P-450، يتم تحويل السيكلوفوسفان إلى مستقلب الخردل فوسفاراميد، الذي له نشاط مضاد للأورام.
قياسًا على السيكلوفوسفاميد، فإن إعطاء 5-فلورويوراسيل داخل الصفاق، والذي يتحول فقط في الكبد إلى 5-فلورو-2-ديوكسيوريدين أحادي الفوسفات (FdUMP)، الذي له نشاط مضاد للأورام، لا معنى له.
اليوم لا توجد معلومات تفيد بأن إعطاء الأدوية المضادة للأورام المساعدة داخل الصفاق بعد العمليات الجذرية يحسن نتائج العلاج. إن مؤشر إعطاء تثبيط الخلايا داخل الصفاق هو تراكم الاستسقاء الناجم عن انتشار الورم في جميع أنحاء الصفاق، من أجل إيقاف أو تقليل معدل تراكمه. قبل إعطاء الأدوية، يجب إزالة الاستسقاء قدر الإمكان ويجب إعطاء الأدوية المضادة للأورام المخففة في 100-200 مل من محلول كلوريد الصوديوم متساوي التوتر.
مخاطر العلاج الكيميائي لدى مرضى سرطان المعدة
العلاج الكيميائي لسرطان المعدة محفوف بمضاعفات خطيرة بسبب سمية الأدوية المضادة للسرطان نفسها وخصائص مسار المرض. على وجه الخصوص، مع سرطان المعدة، هناك فقدان في وزن الجسم، والذي ينبغي أن يؤخذ في الاعتبار عند التخطيط للعلاج الكيميائي. يعد الفقدان السريع لوزن الجسم خلال الشهر الماضي أو الخسارة الإجمالية لأكثر من 10٪ من الوزن الأولي عاملاً غير مواتٍ للغاية. في مثل هؤلاء المرضى، يكون العلاج الكيميائي معقدًا بسبب تطور قلة العدلات العميقة والحموية في كثير من الأحيان، والإنتان، والتهاب الفم، والتهاب الأمعاء والقولون، مصحوبًا بإسهال شديد. عند اختيار العلاج الكيميائي في هؤلاء المرضى، يجب إعطاء الأفضلية للمجموعات الخالية من البلاتين، مما يقلل من جرعات الدواء بنسبة 25-50٪ بالفعل خلال الدورة الأولى.
المظهر الشديد لسوء التغذية هو عسر البلع الشديد أو الكامل بسبب التضيق أو رفض تناول الطعام بسبب "النفور" منه. لا ينبغي إعطاء العلاج الكيميائي للمريض "الجائع". من الضروري أولاً حل التضيق وتحقيق استقرار وزن جسم المريض، ومن ثم التخطيط للعلاج الكيميائي. يجب أن يتلقى المرضى الذين يعانون من فقدان الوزن بسبب العلاج الكيميائي التغذية بالحقن. لتحفيز الشهية، يوصف Megace في قسمنا بجرعة 240-320 ملغ عن طريق الفم يوميًا. تعتبر زيادة الوزن أثناء العلاج الكيميائي مؤشرا هاما على فعاليته، في حين أن فقدان الوزن غالبا ما يكون أول أعراض فشل العلاج.
هناك خطر آخر أثناء العلاج الكيميائي وهو النزيف من ورم أولي غير قابل للإزالة في المعدة أو الانتكاس في منطقة مفاغرة. تشكل هذه المضاعفات تهديدًا لحياة المريض وغالبًا ما تصاحب العلاج الكيميائي الناجح بسبب تفكك الورم. عند إجراء العلاج الكيميائي في المرضى الذين يعانون من آفة أولية غير قابلة للإزالة أو انتكاسة في المعدة، يجب مراقبة مستويات الهيموجلوبين بعناية على الأقل 2-3 مرات في الأسبوع. يجب تحذير المريض من احتمالية الإصابة بالميلينا أو القيء بجلطات الدم وضرورة إخطار الطاقم الطبي على الفور في هذه الحالة. إذا ظهرت علامات النزيف، فيجب إيقاف العلاج الكيميائي، ويجب تركيز كل الجهود على علاج مرقئ الأعراض، بما في ذلك استبدال الدم. بعد توقف النزيف، يجب أن يستمر العلاج الكيميائي فقط على خلفية العلاج المرقئ.
في كثير من الأحيان، يكون النزيف الناتج عن ورم المعدة المتحلل مؤشرًا لاستئصال المعدة الملطف أو استئصال المعدة. إذا جاء
في حالة المريض الشاب الذي تكون حالته مرضية بشكل عام، يكون النزيف الناتج عن ورم المعدة المتحلل مؤشرًا للعلاج الجراحي قبل بدء العلاج الكيميائي.
خاتمة
نجاح العلاج الكيميائي لسرطان المعدة متواضع. إن الحاجة إلى البحث عن أدوية جديدة فعالة مضادة للأورام ومجموعاتها واضحة. إن تحديد الخصائص الجزيئية للخلايا السرطانية السرطانية في المعدة سيحدد أهدافًا جديدة للعمل المستهدف للأدوية التي تمنع مستقبلات عامل النمو ومسارات نقل الإشارات التكاثرية، مما يؤثر على آليات التحكم في دورة الخلية والحفاظ على سلامة الجينوم، وتثبيط تكوين الأوعية الدموية للورم. إن ظهور أنظمة فعالة لعلاج الأشكال النقيلية لسرطان المعدة سوف يبرر استخدامها في المراحل المبكرة من المرض كعلاج مساعد ومساعد.
الأدب
1. فان دي فيلدي ك. العلاج الجراحي والأدوية لسرطان المعدة القابل للجراحة: نتائج تجربتين عشوائيتين للمجموعة الهولندية لسرطان المعدة. مواد المؤتمر الروسي السنوي الثاني للأورام، م، 8-10 ديسمبر 1998 - م، 1999. - ص 43-44.
2. ألوم دبليو إتش، هاليسي إم تي، كيلي كيه إيه. العلاج الكيميائي المساعد في سرطان المعدة القابل للجراحة: متابعة لمدة 5 سنوات لأول تجربة لمجموعة سرطان المعدة البريطانية // لانسيت. - 1989. -المجلد. 1.- ص571-574.
3. بازين آي. إس.، جارين إيه. إم.، زاركوف إس. إيه. الاستجابة للمجموعات المعتمدة على السيسبلاتين في المرضى الذين يعانون من سرطان المعدة المتقدم. المؤتمر الدولي الثاني لعلم الأحياء والوقاية والعلاج من أمراض الجهاز الهضمي الخبيثة. - كولن، 1995. -PP.56.
4. كوكوني جي، كارليني بي، جامبوني إيه وآخرون. PELF أكثر نشاطًا من سرطان المعدة النقيلي FAMTXin (MGC) // Proc. أسكو-2001.
المجلد. 20. - (الملخص 501).
5. كومبس آر سي، شين بي إس، تشيلفرز سي.إي. وآخرون. تجربة عشوائية تقارن المواد المساعدة فلورويوراسيل، ودوكسوروبيسين، وميتوميسين مع عدم وجود علاج في سرطان المعدة القابل للجراحة. المجموعة الدولية للسرطان التعاونية // J. كلين. أونكول. - 1990. - المجلد. 8. - ص 1362-1370.
6. كولينان إس، مورتل سي، فليمنج تي وآخرون. مقارنة بين ثلاثة أنظمة علاج كيميائي في علاج سرطان البنكرياس والمعدة المتقدم// JAMA.. - 1985. - المجلد. 253. - ص2061-2067.
7. دي بارتولوميو إم، باجيتا إي، بوردوجنا جي وآخرون. تحسين النتائج العلاجية المساعدة لدى مرضى سرطان المعدة المستأصلين وفقًا لتورط العقدة: نتائج دراسة عشوائية مدتها 5 سنوات أجرتها التجارب الإيطالية في علم الأورام الطبي (ITMO) // Proc. أسكو. -2000. - المجلد. 19.- الملخص.
934.
8. دوكرو إم، نوردينر بي، يتشو إم وآخرون. سرطان غدي معدي مستأصل: تجربة عشوائية للعلاج الكيميائي المساعد مع 5FU-cisplatyin // المرجع نفسه. - ملخص. 932.
9. إيفانز تي، بول جيه، ماكينيس إيه وآخرون. دراسة المرحلة الأولى وPK للكابيسيتابين بالاشتراك مع الإيبيروبيسين والسيسبلاتين في المرضى الذين يعانون من سرطان غدي مريئي معدي متقدم // المرجع نفسه. -2001. -المجلد. 20.- الملخص. 651.
10. Fielding J.، Scholefield .J، Stuart R. دراسة عشوائية مزدوجة التعمية مضبوطة بالغفل عن الماريماستات في المرضى الذين يعانون من سرطان غدي معدي غير صالح للعمل // المرجع نفسه - 2000. - المجلد. 19.- الملخص. 929.
11. هاليسي إم تي، دان جيه إيه، وارد إل سي، ألوم دبليو إتش التجربة الثانية للمجموعة البريطانية لسرطان المعدة للعلاج الإشعاعي المساعد أو العلاج الكيميائي في سرطان المعدة القابل للاستئصال: متابعة لمدة خمس سنوات // - لانسيت. - 1994. - المجلد. 343 - ص 1309.
12. كانغ واي كيه، تشوي دي دبليو، إيم واي إتش وآخرون. مقارنة عشوائية للمرحلة الثالثة للعلاج الكيميائي المساعد الجديد تليها الجراحة مقابل الجراحة لسرطان المعدة المتقدم محليًا // Proc ASCO. - 1996. - المجلد. 15. - ص215.
13. كاربيه إم إس، كيلسن دي بي، تيبر جي إي. سرطان المعدة // السرطان: مبادئ وممارسة علم الأورام. - نيويورك: ليبينكوت ويليامز وويلكينز، 2001. - ص 1092-1126.
14. كيلسن د.، عتيق أو.، سالتز إل. وآخرون. FAMTX (فلورويوراسيل، ميثوتريكسات، أدرياميسين) فعال وأقل سمية من EAP (إيتوبوسيد، أدرياميسين، سيسبلاتين): تجربة عشوائية في سرطان المعدة // Proc ASCO. - 1991. - المجلد. 10. - ص137.
15. كيم إن كيه، بارك واي إس، هيو دي إس، وآخرون. دراسة عشوائية للمرحلة الثالثة لـ 5 فلورويوراسيل وحده في علاج سرطان المعدة المتقدم // السرطان (فيلاد). - 1993. - المجلد. 71(12). - ص3813.
16. كيم إس، يول إتش، شين إف وآخرون. تجربة المرحلة الثانية من الإبيروبيسين (E)، والسيسبلاتين (P)، وUFT عن طريق الفم، والليكوفورين (L) في مرضى سرطان المعدة المتقدم (AGC). برنامج وملخصات المؤتمر الخامس والعشرين للجمعية الأوروبية لطب الأورام؛ 13-17 أكتوبر 2000؛ هامبورغ، ألمانيا. - ملخص. 274.
17. ماكدونالد جيه، شين بي، وولي بي وآخرون. 5-العلاج الكيميائي المركب بالفلورويوراسيل والدوكسوروبيسين والميتوميسين (FAM) لسرطان المعدة المتقدم // آن. المتدرب. ميد. - 1980. - المجلد. 93. - ص533-536.
18. ماكدونالد جي دي، سمول إس، بينيديتي جيه وآخرون. العلاج الإشعاعي والكيميائي المشترك بعد العملية الجراحية ويحسن البقاء الخالي من الأمراض (DFS) والبقاء الإجمالي (OS) في سرطان غدي مستأصل في المعدة وموصل GE: نتائج دراسة الاندماج INT-0116 (SWOG9008)/
/بروك. أسكو. - 2000. - المجلد. 19.- الملخص. 1.
19. ناكاجيما تي، ناشيموتو أ، كيتامورا إم وآخرون. ميتوميسين مساعد وفلورويوراسيل متبوعًا باليوراسيل عن طريق الفم بالإضافة إلى تيغافور في سرطان المعدة السلبي المصلي: تجربة عشوائية. مجموعة الدراسات الجراحية لسرطان المعدة // لانسيت. - 1999. - المجلد. 354. - ص273.
20. بانزيني آي، جياني إل وآخرون. العلاج الكيميائي المساعد وسرطان المعدة: التحليل التلوي لـ 17 تجربة عشوائية. برنامج وملخصات المؤتمر الخامس والعشرين للجمعية الأوروبية لطب الأورام؛ 13-17 أكتوبر 2000؛ هامبورغ، ألمانيا. - ملخص. 273.
21. بوزو سي، بوجات آر، بيشيل سي وآخرون. Irinotecan بالاشتراك مع CDDP أو 5-FU وحمض الفولينيك نشط في المرضى الذين يعانون من سرطان غدي متقدم في المعدة أو المريء: النتائج النهائية للمرحلة العشوائية IIstudy // Proc. أسكو. - 2001، - المجلد. 20.- الملخص.
531.
22. ريدويلسكي ك.، جيباور تي.، فالكي جيه وآخرون. الجمع بين العلاج الكيميائي مع الدوسيتاكسيل والسيسبلاتين لعلاج سرطان المعدة المتقدم والمنتشر محليًا // آن. أونكول. - 2001. - المجلد. 12. - ص47-51.
23. فان كوتسيم إي جي دي، أجاني جيه، تجولادين إس وآخرون. دوسيتاكسيل بالاشتراك مع سيسبلاتين مع أو بدون 5 فلورويوراسيل في المرضى الذين يعانون من سرطان غدي معدي أو تقاطع GE المتقدم: النتائج الأولية. برنامج وملخصات المؤتمر الخامس والعشرين للجمعية الأوروبية لطب الأورام؛ 13-17 أكتوبر 2000؛ هامبورغ، ألمانيا. - ملخص. 276.
24. فانهوفر يو، روجير بي، ويلك إتش وآخرون. النتائج النهائية لتجربة عشوائية من المرحلة الثالثة للجرعة العالية المتسلسلة من الميثوتريكسيت والفلورويوراسيل والدوكسوروبيسين مقابل إيتوبوسيد وليوكوفورين وفلورويوراسيل مقابل حقن الفلورويوراسيل والسيسبلاتين في سرطان المعدة المتقدم: تجربة المنظمة الأوروبية لأبحاث وعلاج سرطان الجهاز الهضمي السرطاني المجموعة التعاونية للسرطان // J. كلين. أونكول. - 2000.
المجلد. 18. - ص2648-2657.
25. ويب أ.، كننغهام د.، سكارفي ج.ف. وآخرون. تجربة عشوائية تقارن الإيبيروبيسين والسيسبلاتين والفلورويوراسيل مقابل الفلورويوراسيل والدوكسوروبيسين والميثوتريكسيت في سرطان المريء المعدي المتقدم // المرجع نفسه. - 1997. - المجلد. 15. - 261-267.
26. ويلس ج.، كلاين ه.، فاغنر د. وآخرون. جرعة عالية متتابعة من الميثوتريكسيت والفلورويوراسيل مع دوكسوروبيسين: خطوة إلى الأمام في علاج سرطان المعدة المتقدم - تجربة المجموعة التعاونية للجهاز الهضمي EORTC // المرجع نفسه. - 1991. - المجلد. 9. - ص 827-831.
27. ويلس ج. علاج سرطان المعدة المتقدم // سيمين. أونكول. - 1996. - المجلد. 23. - ص397-403.
علم الأورام العملي
سي.أ. تيلاندين
المرفق 1.
تركيبات تستخدم لعلاج سرطان المعدة
مألوف
- 5-فلورويوراسيل 600 ملجم/م2 أيام 1، 8، 29، 36
- دوكسوروبيسين 30 ملغم/م2 عن طريق الوريد الأيام 1، 29
- Mitomycin-C 10 mg/m2 اليوم الأول تكرر الدورة كل 8 أسابيع. فامتكس
- الميثوتريكسيت 1500 ملغم/م2 بالتسريب لمدة 30 دقيقة يومياً 1
- 5-فلورويوراسيل 1500 ملغم/م2 تسريب 30 دقيقة بعد ساعة من تناول الميثوتريكسيت
- ليوكوفورين 30 ملغ عن طريق الوريد أو الفم بعد 24 ساعة من الميثوتريكسيت كل 6 ساعات 8 جرعات
- دوكسوروبيسين 30 ملغم/م2 وريدياً في اليوم 15. دورة علاجية متكررة في اليوم 22.
EAP
- إيتوبوسيد 120 ملغم/م2 عن طريق الوريد في الأيام 4، 5، 6
- دوكسوروبيسين 20 ملغم/م2 عن طريق الوريد في اليوم الأول والسابع
- سيسبلاتين 40 ملغم/م2 عن طريق الوريد في اليومين الثاني والثامن. دورة علاجية متكررة في اليوم 29.
- سيسبلاتين 100 ملغم/م2 عن طريق الوريد، اليوم الأول
- فلورويوراسيل بجرعة يومية 1000 ملغم / م 2 بالتسريب في الوريد 1-5 أيام يتم العلاج كل 28 يومًا.
قزم
- إيتوبوسيد 120 ملغم/م2 عن طريق الوريد في الأيام 1، 2، 3
- ليوكوفورين 30 ملغم/م2 عن طريق الوريد في الأيام 1، 2، 3
- 5-فلورويوراسيل 500 ملغم/م2 بلعة في الوريد 1، 2، 3 أيام. يتكرر مسار العلاج في اليوم 28.
ثروة
- سيسبلاتين 40 ملغم/م2 عن طريق الوريد في اليومين الأول والخامس؛
- الإبيروبيسين 30 ملغم/م2 عن طريق الوريد في اليومين الأول والخامس
- ليوكوفورين 100 ملغم/م2 وريدياً 1-4 أيام
- 5-فلورويوراسيل 300 ملغم/م2 وريدياً 1-4 أيام علاج كل 4 أسابيع.
ECF
- إبيروبيسين 50 ملغم/م2 وريدياً كل 3 أسابيع
- سيسبلاتين 60 ملغم/م2 وريدياً كل 3 أسابيع
- 5-فلورويوراسيل بجرعة يومية قدرها 200 ملغم/م2 بالتسريب الوريدي المستمر خلال الأسبوع 18-21 من TC
- سيسبلاتين 75 ملغم/م2 عن طريق الوريد اليوم الأول تكرر الدورة كل 3 أسابيع
- دوسيتاكسيل 75 ملغم/م2 عن طريق الوريد اليوم الأول
- سيسبلاتين 75 ملغم/م2 عن طريق الوريد اليوم الأول
- 5- فلورويوراسيل بجرعة يومية 750 ملغم/م2 تسريب في الوريد في الأيام 1-5، وتجرى دورة العلاج كل 3 أسابيع.
- إرينوتيكان 200 ملغم/م2 عن طريق الوريد، اليوم الأول
- سيسبلاتين 60 ملغم/م2 عن طريق الوريد اليوم الأول علاج كل 3 أسابيع
اذا كنت
- إرينوتيكان 80 ملغم/م2
- ليوكوفورين 500 مجم/م2 2 ساعة
- 5-فلورويوراسيل 2000 ملغم/م2 يتم تسريبه على مدار 22 ساعة أسبوعياً لمدة 6 أسابيع، ويتكرر بعد فترة أسبوعية. الهندسة الكهربائية والميكانيكية
- ميتوميسين 5 ملغم/م2 عن طريق الوريد في اليوم الأول والسابع
- إيتوبوسيد 60 ملغم/م2 عن طريق الوريد في الأيام 4، 5، 6
- سيسبلاتين 40 ملغم/م2 عن طريق الوريد في اليومين الثاني والثامن. دورة علاجية كل 4 أسابيع.
العلاج الكيميائي هو وسيلة لعلاج الأورام التي تستخدم أدوية تثبيط الخلايا (مضادة للورم).
في كثير من الأحيان يتم استخدام النهج النظامي، حيث تدخل الأدوية إلى مجرى الدم وتنتشر في جميع أعضاء الجسم، مما يؤدي إلى تدمير الخلايا المرضية. لكن العلاج الكيميائي الموضعي يستخدم أيضًا، عندما يتم علاج مناطق معينة من الجسم.
يقدم مستشفى أساف هروفيه خدمات العلاج الكيميائي لعلاج السرطان. هذه هي أكبر مؤسسة طبية عامة في إسرائيل. هنا، سيتمكن المريض الأجنبي من الحصول على رعاية طبية تلبي أعلى المعايير الدولية.
قم بالتسجيل للحصول على استشارة
العلاج الكيميائي لسرطان المستقيم في إسرائيل
يتم علاج سرطان المستقيم بالعوامل المثبطة للخلايا في قسم الأورام في آساف:
قبل الجراحة مع أو بدون إشعاع لتقليل حجم الورم. وهو مفيد بشكل خاص عندما يقع الورم الخبيث بالقرب من العضلة العاصرة الشرجية. إذا أدى التعرض لمثبطات الخلايا إلى تقليل تورم المستقيم، فقد يحافظ الطبيب على العضلة العاصرة.
بعد الجراحة، مع أو بدون العلاج الإشعاعي، يتم تدمير الأجزاء المرضية المتبقية وتقليل خطر تكرار المرض. تقليل مظاهر عملية الورم النقيلي. وهنا يتم استخدام العلاج الكيميائي لسرطان القولون والمستقيم كوسيلة علاجية رئيسية عند ظهور آفات ثانوية في الكبد أو الرئتين، وذلك من أجل السيطرة على المرض لأطول فترة ممكنة.
الأدوية الرئيسية المستخدمة لتثبيط الخلايا:
- فلورويوراسيل (5-FU) - يُعطى كحقن في الوريد، بشكل متقطع أو بالتسريب المستمر؛
- Xeloda® (أقراص)؛
- إرينوتيكان* (عن طريق الوريد)؛
- رالتيتريكسيد (عن طريق الوريد).
أنظمة العلاج الكيميائي لسرطان المستقيم:
- 5-FU وليوكوفورين (فولينات الكالسيوم).
- يزيد الليوكوفورين من فعالية 5-FU.
- FOLFOX – إلوكساتين بالاشتراك مع 5-FU وليوكوفورين.
- يستخدم هذا النظام أيضًا مع بيفاسيزوماب.
- FOLFIRI - إرينوتيكان بالاشتراك مع 5-FU وحمض الفوليك.
- يتم إعطاء FOLFIRI أيضًا مع Avastin.
- فولفوكسيري - إرينوتيكان، أوكساليبلاتين، 5-FU وحمض الفوليك.
- يتم وصف Irinotecan وcapecitabine أيضًا مع Avastin.
- يمكن دمج أوكساليبلاتين وكابيسيتابين مع أفاستين.
إذا لم تحقق أدوية علاج الخط الأول التأثير المطلوب، يستخدم الأطباء عوامل تثبيط الخلايا الأخرى:
- يُعطى سيتوكسيماب (إربيتوكس)، وهو دواء علاجي مستهدف، جنبًا إلى جنب مع إرينوتيكان ويوصف عند فشل العلاج الأولي أو الثانوي.
- يتم تحديد استخدام سيتوكسيماب من خلال الأدوية التي تم استخدامها كعلاج أولي وما إذا كان الاختبار الجيني إيجابيًا لطفرات جين KRAS.
- إذا تم العثور على طفرات، لا يوصف سيتوكسيماب، حيث أن تأثيره موجه نحو مستقبلات عامل نمو البشرة EGFRs. أنها تعزز تطوير الخلايا المرضية.
- Panitumumab (Vectibix) هو علاج مستهدف لعلاج سرطان القولون والمستقيم النقيلي الذي تم علاجه سابقًا باستخدام 5-FU، أو irinotecan، أو oxaliplatin.
احصل على استشارة الطبيب
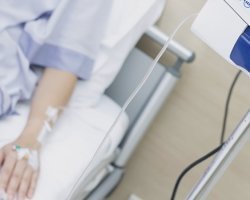 يُسمى هذا النوع من العلاج المثبط للخلايا بالمساعد. الهدف من العلاج هو المساعدة في منع السرطان من العودة أو الانتشار إلى أجزاء أخرى من الجسم. أثناء العملية، سوف يرى الجراح مدى عمق نمو السرطان في جدار الأمعاء أو الأنسجة المحيطة به، ويحدد حجم الورم. يتم إرسال العينات إلى المختبر لمزيد من الدراسة.
يُسمى هذا النوع من العلاج المثبط للخلايا بالمساعد. الهدف من العلاج هو المساعدة في منع السرطان من العودة أو الانتشار إلى أجزاء أخرى من الجسم. أثناء العملية، سوف يرى الجراح مدى عمق نمو السرطان في جدار الأمعاء أو الأنسجة المحيطة به، ويحدد حجم الورم. يتم إرسال العينات إلى المختبر لمزيد من الدراسة.
العوامل التي تشير إلى احتمالية عودة المرض:
- تم العثور على الخلايا الخبيثة في العقد الليمفاوية التي تمت إزالتها أثناء الجراحة.
- انتشر السرطان إلى الأوعية الدموية (غزو الأوعية الدموية).
- توغلت عملية الورم بعمق في جدار الأمعاء أو أثرت على الأنسجة المحيطة.
في مثل هذه الحالات، تنفصل الخلايا الخبيثة عن الورم الرئيسي في المستقيم وتنتقل عبر مجرى الدم أو الجهاز اللمفاوي. وهي صغيرة جدًا بحيث لا يمكن اكتشاف الخلايا بواسطة التصوير المقطعي، ولكنها لا تزال قادرة على تكوين أورام ثانوية.
يكون العلاج الكيميائي فعالاً إذا كان السرطان صغيرًا وليس كبيرًا. لذلك ينصح الطبيب بالعلاج بمثبطات الخلايا بعد الجراحة لتقليل احتمالية عودتها أو انتشارها. وينتقل الدواء عبر مجرى الدم إلى جميع أنحاء الجسم، ويدمر الخلايا الخبيثة.
يبدأ العلاج الكيميائي بعد حوالي 8 أسابيع، عندما يستعيد المريض وعيه بعد الجراحة.
أدوية العلاج الكيميائي لسرطان المستقيم بعد الجراحة:
- فولفوكس هو مزيج من حمض الفوليك (ليكوفورين)، فلورويوراسيل وأوكسالبلاتين (عن طريق الوريد).
- كابيسيتابين (زيلودا) – في أقراص.
- فلورويوراسيل (5-FU) – عن طريق الوريد.
- XELOX - مزيج من أوكساليبلاتين وكابيسيتابين
قد يكون العلاج مطلوبًا لمدة 6 إلى 7 أشهر. يمكن أن تكون أدوية العلاج الكيميائي على شكل أقراص يمكن تناولها في المنزل. إما أن يكون هذا علاجًا عن طريق الوريد باستخدام قنية أو قسطرة مركزية أو خط القسطرة المركزية المدخلة (PICC) أو المنفذ.
العلاج الكيميائي لسرطان المستقيم المتقدم
العلاج باستخدام تثبيط الخلايا لن ينقذ المريض من سرطان المستقيم المتقدم، لكنه يمكن أن يقلل من عملية الورم ويزيد من فرص البقاء على قيد الحياة. أهداف العلاج هي إبطاء تطور المرض وإدارة أعراضه – الألم، وفقدان الشهية، وفقدان الوزن.
في المراحل المتقدمة من السرطان، الهدف الرئيسي من العلاج هو مساعدة المريض على الشعور بالتحسن. لذلك، إذا كانت الآثار الجانبية شديدة، يتم إيقاف العلاج.
أدوية العلاج الكيميائي المستخدمة لعلاج سرطان القولون والمستقيم المتكرر أو المتقدم:
- كابيسيتابين (زيلودا) (أقراص)
- فلورويوراسيل (5-FU)
- رالتيتريكسيد في الوريد.
- يوصى باستخدام Raltitrexed عندما يكون هناك موانع لاستخدام 5-FU أو capecitabine.
- أوكساليبلاتين
- إرينوتيكان
سيستخدم الأطباء عدة مجموعات مختلفة من هذه الأدوية، بما في ذلك:
- فولفوكس
- فولفيري
- XELOX (أوكسالبلاتين وكابيسيتابين).
عند اختيار الأدوية، يأخذ الطبيب في الاعتبار عوامل مختلفة للعثور على الخيار الأفضل. ويأخذ في الاعتبار العلاج السابق الذي تم تقديمه والمدة التي استغرقها المرض للعودة. يناقش طبيب الأورام خيارات العلاج مع المريض.
إذا عاد السرطان، يتم استخدام مثبطات الخلايا الأخرى، ويسمى العلاج علاج الخط الثاني.
تُجرى التجارب باستمرار لتحسين علاج سرطان القولون والمستقيم المتقدم.
تعرف على تكلفة العلاج
كيف يتم فحص فعالية العلاج الكيميائي لسرطان المستقيم؟
قبل البدء بالعلاج، يقوم الطبيب بإجراء فحص، ثم بعد 3 أشهر. يتم قياس حجم الورم بحيث يمكن تحديد مدى فعالية العلاج مع مرور الوقت. خيارات:
- لقد انخفض الورم الخبيث.
- يبقى بنفس الحجم.
- زيادة.
إذا ظل حجم الورم كما هو، فسيتحدث الطبيب مع المريض حول مواصلة العلاج - سواء كان الأمر يستحق الاستمرار أم لا.
عندما ينخفض أو يبقى كما هو، سيكون العلاج مطلوبًا لمدة 4-6 أشهر أخرى. يستمر العلاج حتى تحدث الكثير من الآثار الجانبية. يتم إيقاف العلاج مؤقتًا. سيتحدث الطبيب عن مزايا وعيوب الخيارات المختلفة. عادة، يتم إجراء الأشعة المقطعية كل 2-3 أشهر لتحديد مدى فعالية العلاج.
إذا أصبح الورم أكبر، سيتم إيقاف العلاج الكيميائي وسيتم التوصية بطريقة أخرى.
العلاج الكيميائي والجراحة لإزالة نقائل الكبد.
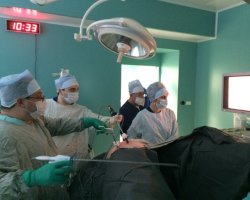 في بعض الأحيان يوصي الأطباء بإجراء عملية جراحية لإزالة الآفات الثانوية في الكبد.
في بعض الأحيان يوصي الأطباء بإجراء عملية جراحية لإزالة الآفات الثانوية في الكبد.
يتم إجراء الجراحة إذا لم تكن هناك علامات أخرى للسرطان في الجسم. للقيام بذلك، يتم إجراء فحص PET-CT للبحث عن الخلايا الخبيثة خارج الكبد.
عندما يكون الورم في الكبد كبيرًا جدًا بحيث لا يمكن إزالته، يوصى بأخذ دورة من العلاج الكيميائي لسرطان المستقيم لتقليل حجم الورم. يتم العلاج باستخدام تثبيط الخلايا قبل الجراحة وبعدها.
إذا كان العلاج الكيميائي القياسي للنقائل غير فعال، يتم تقديم العلاج في التجارب السريرية.
يستخدم العلاج الكيميائي في هذه الحالة:
- تدمير الخلايا السرطانية التي غزت الكبد ولم تتطور إلى أورام.
- من أجل تدمير الأجزاء الخبيثة التي قد تبقى بعد إجراء عملية جراحية لإزالة ورم في الكبد.
- لتقليل حجم الورم الخبيث في الكبد قبل الجراحة، لإتاحة إزالة الورم غير القابل للجراحة.
يتم إعطاء الفلوكسوريدين (FUDR)، وهو دواء مشابه لـ 5-FU، من خلال قسطرة صغيرة توضع في الشريان الكبدي. يتم إعطاء الدواء أيضًا على مدى فترة زمنية أطول باستخدام مضخة مزروعة في منطقة الكبد. يُسمى هذا النوع من العلاج الكيميائي الموضعي لسرطان المستقيم بالتسريب الشرياني الكبدي.
يمكن أيضًا استبدال العلاج بالفلوكسوريدين الموضعي بالعلاج الكيميائي 5-FU الوريدي. تتمثل ميزة العلاج الكيميائي الموضعي في أنه يوفر تركيزًا عاليًا من الأدوية السامة للخلايا للورم وعادةً ما يؤدي إلى تأثيرات غير مرغوب فيها أقل للعلاج في أجزاء أخرى من الجسم. العيب هو عدم التأثير على الخلايا الخبيثة التي قد تكون موجودة خارج حدود هذا العضو.
طلب استدعاء
العلاج الكيميائي لسرطان المستقيم
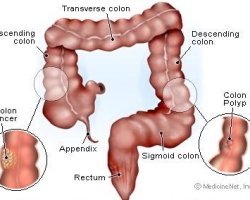 غالبًا ما يتم علاج هذا المرض بالإشعاع قبل الجراحة أو بعدها. تساعد هذه التقنية على منع الانتكاس. يعمل العلاج الإشعاعي على تقليص حجم الورم، مما يجعل إزالته أسهل.
غالبًا ما يتم علاج هذا المرض بالإشعاع قبل الجراحة أو بعدها. تساعد هذه التقنية على منع الانتكاس. يعمل العلاج الإشعاعي على تقليص حجم الورم، مما يجعل إزالته أسهل.
يُستخدم العلاج الكيميائي لسرطان المستقيم أيضًا بالتزامن مع العلاج الإشعاعي. تثبيط الخلايا يجعل الخلايا الخبيثة أكثر حساسية للإشعاع.
نظرًا لأن العلاج عبارة عن علاج مركب، فمن المرجح أن يكون أكثر نجاحًا من العلاج الإشعاعي وحده. في مثل هذه الحالات، يتم استخدام أدوية العلاج الكيميائي - فلورويوراسيل (5-FU)، كابيسيتابين.
5-دخول الFU إلى الجسم:
- باستخدام قطارة.
- من خلال مضخة يرتديها المريض 24 ساعة يوميا.
- كسلسلة من الحقن في الوريد قبل العلاج الإشعاعي.
يأخذ المريض دواء كابيسيتابين على شكل أقراص في الصباح والمساء أثناء العلاج الإشعاعي.
الجمع بين العلاج الإشعاعي والعلاج الكيميائي يزيد من الآثار الجانبية. العلاج المختلط سيزيد من التعب. كما يعاني المريض أحيانًا من الإسهال والغثيان وضعف المقاومة للعدوى وكثرة التبول وتهيج الجلد في منطقة العلاج.
الآثار الجانبية المحتملة بعد العلاج الكيميائي لسرطان القولون والمستقيم
من خلال تدمير الخلايا السرطانية، يقتل العلاج الكيميائي الخلايا السليمة التي تخضع للانقسام والنمو السريع. خلايا الدم، لذا فإن العلاج باستخدام مثبطات الخلايا سيقلل من عدد خلايا الدم البيضاء وخلايا الدم الحمراء والصفائح الدموية. وهذا يعني ما يلي:
- يشعر المريض بالتعب.
- سوف تزيد احتمالية الإصابة.
- يصبح الشخص عرضة لأنواع مختلفة من النزيف.
إذا ارتفعت درجة حرارتك فوق 38 درجة مئوية أو ظهرت عليك علامات العدوى، فمن المهم الذهاب إلى المستشفى على الفور. في بعض الأحيان قد تكون هناك حاجة إلى علاج عاجل بالمضادات الحيوية.
التعب هو التأثير الجانبي الأكثر شيوعًا لدى الأشخاص الذين يخضعون للعلاج الكيميائي. قد يعاني المريض من الضعف ونقص الطاقة. تحدث هذه الحالة لعدة أشهر بعد انتهاء العلاج. تعتمد سرعة عودة الشخص إلى الحياة الطبيعية على الحالة الصحية العامة والعلاج السابق والإجراءات المخطط لها.
تشمل الآثار السلبية المحتملة الأخرى للعلاج الكيميائي ما يلي:
- غثيان؛
- إسهال؛
- التهاب الفم.
- تساقط الشعر أو ترققه.
- التغيرات في الدورة الشهرية.
- ألم في العينين، والشعور كما لو أن الرمل قد سكب فيها.
غالبًا ما يتم استخدام أدوية العلاج الكيميائي التالية لهذا المرض:
- فلورويوراسيل.
- حمض الفوليك؛
- رالتيتريكسيد.
- إرينوتيكان.
- أوكساليبلاتين.
احصل على برنامج علاجي
الآثار الجانبية للفلورواسيل (5-FU)
معظم الناس يتعاملون بشكل جيد مع هذا الدواء وهناك آثار جانبية قليلة، وأكثرها شيوعاً هي:
- غثيان؛
- تعب؛
- إسهال؛
- انخفاض في خلايا الدم الحمراء.
- التهاب الفم.
إذا تم تناول 5-FU من خلال مضخة، يحدث أحيانًا احمرار وألم في اليدين والقدمين - حمامي راحي أخمصي. يحدث في 1 من كل 3 مرضى. تقشر الجلد على راحتي اليدين وأخمص القدمين. في غالبية المرضى، يكون هذا العرض خفيفًا جدًا، ويستمر العلاج. إذا تفاقمت الحالة، سيقوم الطبيب بتقليل جرعة الدواء أو يوصي بأخذ قسط من الراحة حتى يتعافى المريض.
الآثار الجانبية للكابيسيتابين (زيلودا)
الآثار الجانبية للكابيسيتابين تشبه إلى حد كبير تلك الخاصة بـ 5-FU، مما يسبب أيضًا احمرارًا وألمًا في اليدين والقدمين - الحمامي الراحية الأخمصية.
في كثير من الأحيان تكون الأعراض خفيفة؛ إذا ساءت حالة المريض، يتم تقليل جرعة زيلودا أو يقترح أخذ قسط من الراحة حتى يتعافى المريض.
الآثار الجانبية للرالتيتريكسيد (Tomudex)
يوصف هذا المثبط للخلايا لعلاج المرضى عندما لا يكون من الممكن تناول الفلورويوراسيل أو الكابيسيتابين. قد يكون هذا بسبب مشاكل في القلب مثل الذبحة الصدرية.
تشمل الآثار الجانبية الشائعة لـ Tomudex ما يلي:
- انخفاض خلايا الدم.
- الإسهال الذي يحدث بعد أيام قليلة من بدء العلاج.
- يمكن أن يكون التأثير الجانبي خطيرًا جدًا، لذا من المهم إبلاغ طبيبك فورًا.
- تعب.
- غثيان.
- التهاب الفم، بما في ذلك التهاب الحلق وصعوبة التنفس.
- عادة ما تكون التغيرات في وظائف الكبد خفيفة بما يكفي لتسبب الأعراض.
- يقوم الطبيب بإجراء فحوصات دم منتظمة للتحقق من عمل العضو.
- الطفح الجلدي.
- اضطراب في المعدة وألم.
الآثار الجانبية للإرينوتيكان
تشمل العواقب غير المرغوب فيها الشائعة للعلاج الدوائي ما يلي:
- زيادة التعرق.
- تعب.
- عيون دامعة.
- غثيان.
- ترقق أو تساقط الشعر.
- انخفاض خلايا الدم.
- زيادة إنتاج اللعاب.
- ألم تشنجي في البطن.
- إسهال.
يعاني بعض الأشخاص من التعرق وآلام البطن والإسهال أثناء العلاج. وللحد من الآثار الجانبية، يصف الطبيب عقار الأتروبين ويعطي حقنة تحت الجلد.
يمكن أن يكون الإسهال بعد إرينوتيكان من الآثار الجانبية الخطيرة. ويجب عليك إخطار طبيبك في حالة حدوث هذا العرض. في بعض الأحيان سوف تحتاج إلى تناول الأدوية المضادة للإسهال. قد يصف طبيبك مضادًا حيويًا إذا تفاقم الإسهال. في بعض الأحيان، يبدأ الجفاف بسرعة كبيرة، لذا يجب عليك الاتصال بطبيبك على الفور.
الآثار الجانبية للأوكساليبلاتين
تشمل الآثار غير المرغوب فيها الشائعة للعلاج ما يلي:
- غثيان؛
- خدر الشفاه.
- حساسية للبرد.
- تنميل ووخز في اليدين والقدمين.
يحدث التنميل والوخز بسبب تأثير عقار أوكساليبلين على الأعصاب. يستمر الشعور بالبرد لعدة أيام بعد تناول الدواء. في بعض الأحيان، تصبح الأعراض مشكلة أكثر خطورة إذا استمر العلاج بالدواء لفترة كافية. أفاد بعض الأشخاص أنهم يجدون صعوبة في المشي بسبب خدر باطن أقدامهم.
يجب عليك إخبار طبيبك في حالة حدوث وخز أو تنميل، خاصة إذا لم تزول هذه الأعراض. يجب تقليل جرعة الدواء أو إيقاف العلاج مؤقتًا. يمكن استخدام أدوية العلاج الكيميائي الأخرى. بالنسبة لبعض الناس، يصبح هذا التأثير الجانبي دائمًا.
قم بالتسجيل للحصول على العلاج
|
مرحلة العلاج الكيميائي |
||
|
شديد |
استمرار |
|
|
4**** ح ر* / 4 ح 3 ر 3 * 6 ح ر** / 6 ح 3 ر 3 ** 6 ح ز *** / 6 ح 3 ض 3 ه 3 *** |
||
|
2 H R Z E S + 1 H R Z E |
5 ح ر ه / 5 ح 3 ص 3 ه 3 6 ح ر *** / 6 ح 3 ر 3 ه 3 *** |
|
|
3 ح ر ز ه /[ك] |
وفقًا للأنظمة I أو IIa أو IV، اعتمادًا على حساسية المتفطرات للدواء |
|
|
4 ح ر/ 4 ح 3 ص 3 |
||
|
ما لا يقل عن 5 أدوية يتم الحفاظ على الحساسية لها مدة المرحلة لا تقل عن 6 أشهر |
ما لا يقل عن 3 أدوية يتم الحفاظ على الحساسية لها مدة المرحلة لا تقل عن 12 شهرا |
|
ملحوظات
* لمرض السل التنفسي
** لمرض السل خارج الرئة، لمرض السل بأي شكل من الأشكال لدى الأطفال والمراهقين
*** لعلاج مرض السل بأي شكل من الأشكال لدى الأطفال والمراهقين
**** مدة دورة العلاج الكيميائي بالأشهر
الاختصارات:ح– أيزونيازيدر– ريفامبيسين،ز– بيرازيناميد،ه– إيثامبوتول،س– الستربتوميسين،روبية- ريفابوتين،ك- كاناميسين / أميكاسين،نقطة- بروثيوناميد،قبعة– كابريوميسين،فق- أدوية من مجموعة الفلوروكينولونات،خدمات العملاء– السيكلوسيريننظام تقييم الأداء- باسك
تتم الإشارة إلى الخيارات الممكنة للأنظمة وإدراج الأدوية الفردية فيها بعد علامة "/". بين قوسين معقوفين يتم إعطاء الأنظمة والأدوية، التي تعتمد الوصفة الطبية عليها على بيانات عن حساسية الدواء للبكتيريا.
3.1. أولاً (أنا) نظام العلاج الكيميائييوصف للمرضى الذين تم تشخيصهم حديثًا والذين يعانون من إفراز بكتيري و/أو تلف واسع النطاق أو معقد لمختلف الأعضاء.
في مرحلة العناية المركزةيتم وصف 4 أدوية رئيسية: أيزونيازيد، وريفامبيسين، وبيرازيناميد، وستربتومايسين أو إيثامبوتول. من الأفضل وصف هذا الأخير في المناطق ذات المقاومة المتكررة لبكتيريا المتفطرة السلية للستربتوميسين 1. تستمر المرحلة المكثفة من العلاج الكيميائي لمدة شهرين على الأقل. خلال هذه الفترة، يجب على المريض تناول 60 جرعة من مزيج من 4 أدوية رئيسية. في حالة تفويت الجرعات الكاملة، يتم زيادة مدة مرحلة العلاج المكثف إلى 60 جرعة.
بعد شهرين من بداية العلاج، يتم تحديد مسألة الانتقال إلى المرحلة الثانية من قبل لجنة الخبراء السريرية (CEC) بناءً على بيانات الدراسات السريرية والإشعاعية والميكروبيولوجية.
إذا استمر إفراز البكتيريا (كما هو محدد بواسطة الفحص المجهري للبلغم) بعد شهرين من العلاج الكيميائي، فيمكن أن تستمر مرحلة العلاج المكثف لمدة شهر آخر (30 جرعة) حتى يتم الحصول على بيانات حول حساسية الدواء للعامل الممرض. اعتمادا على النتيجة، يتم تعديل العلاج الكيميائي وتستمر مرحلة العلاج المكثف (بقرار من اللجنة الاقتصادية الأوروبية). إذا كان من المستحيل دراسة حساسية الدواء و/أو إذا كانت الديناميكيات السريرية والإشعاعية للعملية سلبية بعد 3 أشهر من العلاج الكيميائي، يتم إرسال المريض إلى مؤسسة عليا لدراسة حساسية الدواء وتحديد أساليب الإدارة الإضافية. أثناء انتظار النتائج، يتم العلاج وفقًا للمرحلة المكثفة من العلاج.
في حالة مرض السل الشديد والمعقد بأي شكل من الأشكال، يمكن زيادة مدة مرحلة العلاج المكثف وفقًا لقرار اللجنة الاقتصادية الأوروبية.
إذا كانت نتائج الفحص المجهري للبلغم سلبية بعد شهرين من العلاج الكيميائي وكانت الديناميكيات السريرية والإشعاعية إيجابية، فسيتم الانتقال إلى مرحلة استمرار العلاج الكيميائي.
في مرحلة الاستمراريتم وصف دواءين رئيسيين - أيزونيازيد وريفامبيسين - لمدة 4 أشهر (لمرض السل التنفسي) أو لمدة 6 أشهر (للسل خارج الرئة) يوميًا أو بشكل متقطع مرتين (3 مرات في الأسبوع). وهناك نظام آخر في مرحلة الاستمرار يمكن أن يكون أيزونيازيد وإيثامبوتول يوميًا لمدة 6 أشهر. بالنسبة لالتهاب السحايا السلي لدى البالغين، تستمر مرحلة العلاج المستمرة من 8 إلى 12 شهرًا.
يتم وصف الأطفال والمراهقين في مرحلة استمرار العلاج لمدة 6 أشهر. أيزونيازيد وريفامبيسين أو أيزونيازيد وبيرازيناميد وإيثامبوتول يومياً أو بشكل متقطع (3 مرات في الأسبوع). يمكن تمديد مرحلة الاستمرار إلى 9 أشهر عند الأطفال والمراهقين المصابين بالسل المعمم والتهاب السحايا السلي، مع استمرار تدمير أنسجة الرئة لأكثر من 6 أشهر دون إفراز بكتيري، وكذلك في الأطفال دون سن 3 سنوات من العمر. يمكن لهؤلاء المرضى تلقي 3 أدوية في مرحلة الاستمرار: أيزونيازيد وريفامبيسين وبيرازيناميد أو إيثامبوتول.
3.2. الثاني أ(ثانياأ) وضعيوصف العلاج الكيميائي لدورة ثانية من العلاج الكيميائي بعد انقطاع العلاج أو للانتكاس مع انخفاض خطر مقاومة الأدوية من المتفطرة السلية.
في مرحلة العناية المركزةتوصف 5 أدوية رئيسية: أيزونيازيد، وريفامبيسين، وبيرازيناميد، وإيثامبوتول، وستربتومايسين. بعد شهرين (يتم تناول 60 جرعة يومية)، يستمر العلاج بأربعة أدوية (أيزونيازيد، ريفامبيسين، بيرازيناميد، إيثامبوتول) لمدة شهر آخر (30 جرعة). المدة الإجمالية للمرحلة المكثفة هي 3 أشهر على الأقل (90 جرعة يومية من تركيبة الدواء). في حالة تفويت الجرعات الكاملة، يتم زيادة مدة المرحلة المكثفة إلى 90 جرعة.
في 3 أشهر. منذ بداية مرحلة العلاج المكثف، يتم تحديد مسألة الانتقال إلى المرحلة الثانية من العلاج من قبل لجنة الانتخابات المركزية بناءً على بيانات الفحص السريري والإشعاعي والميكروبيولوجي.
إذا استمر إفراز البكتيريا وكان من المستحيل دراسة حساسية المتفطرة السلية للدواء و/أو إذا كانت الديناميكيات السريرية والإشعاعية للعملية سلبية، يتم إرسال المريض بعد 3 أشهر إلى مؤسسة عليا لدراسة حساسية الدواء وتحديد المزيد من الإدارة التكتيكات. حتى يتم الحصول على النتائج، يتم العلاج كما هو الحال في المرحلة المكثفة من العلاج.
إذا كانت نتائج الفحص المجهري للبلغم سلبية بعد 3 أشهر من العلاج الكيميائي وكانت الديناميكيات السريرية والإشعاعية إيجابية، تبدأ مرحلة استمرار العلاج الكيميائي. بحلول هذا الوقت، كقاعدة عامة، يتم الحصول على بيانات عن حساسية الدواء لمرض السل المتفطرة، والتي قد تتطلب تصحيح العلاج الكيميائي.
إذا كانت المتفطرة السلية حساسة لأدوية العلاج الكيميائي الرئيسية مرحلة الاستمرارلمدة 5 أشهر أخرى، يتم وصف الإيزونيازيد والريفامبيسين والإيثامبوتول يوميًا أو بشكل متقطع. 1 الوضع (3 مرات في الأسبوع). المدة الإجمالية للعلاج هي 8 أشهر. بالنسبة للأطفال والمراهقين، تستمر مرحلة العلاج لمدة 6 أشهر، وتكون المدة الإجمالية للعلاج 9 أشهر.
3.3. الوضع الثاني B (II b).يوصف العلاج الكيميائي للمرضى الذين يعانون من مخاطر عالية لمقاومة المتفطرات للأدوية حتى يتم الحصول على نتائج الدراسة الميكروبيولوجية. وتشمل هذه:
المرضى الذين ليس لديهم أي تأثير للعلاج الكيميائي أو لديهم تفاقم أو تقدم في العملية أثناء العلاج؛
المرضى الذين لم يتلقوا من قبل أدوية مضادة للسل، ولكن لديهم سبب وجيه للاشتباه في مقاومة الأدوية بناءً على البيانات السابقة للذاكرة و/أو السريرية (الاتصال بالمرضى الذين يفرزون المتفطرة السلية المقاومة للأدوية المتعددة، مسار تقدمي حاد).
في مرحلة العناية المركزة لمدة 3 أشهر، يتم وصف مزيج من 4 أدوية رئيسية (إيزونيازيد، وريفامبيسين/ريفابوتين، وبيرازيناميد، وإيثامبوتول) و2-3 أدوية احتياطية (اعتمادًا على بيانات مقاومة الأدوية في المنطقة).
يتم ضبط العلاج الإضافي بناءً على البيانات المتعلقة بحساسية المتفطرة السلية للدواء ويتم إجراؤه وفقًا للأنظمة الأولى (I) أو الثانية A (II a) أو الرابعة (IV).
يمكن استخدام نظام العلاج هذا في مؤسسات مكافحة السل التي لديها خدمة مختبرية مع آلية مراقبة الجودة الحالية والقدرة على تحديد مقاومة الأدوية للأدوية الاحتياطية.
3.4. ثالث (ثالثا) وضعيوصف العلاج الكيميائي للمرضى الذين تم تشخيصهم حديثًا دون إفراز البكتيريا، والذين يعانون من أشكال بسيطة (محدودة) وغير معقدة من مرض السل.
في مرحلة العناية المركزةيتم وصف 4 أدوية رئيسية: أيزونيازيد، ريفامبيسين، بيرازيناميد، إيثامبوتول. يوصف للأطفال 3 أدوية رئيسية: أيزونيازيد وريفامبيسين وبيرازيناميد أو ستربتومايسين أو إيثامبوتول (لا يوصف الأخير لأطفال ما قبل المدرسة). تستمر المرحلة المكثفة لمدة شهرين. خلال هذه الفترة، يجب على المريض تناول 60 جرعة من مزيج من 4 أدوية رئيسية (عند الأطفال - 3). في حالة تفويت الجرعات الكاملة، يتم زيادة مدة مرحلة العلاج المكثف إلى 60 جرعة.
بعد شهرين من بداية المرحلة المكثفة من العلاج، يتم تحديد مسألة الانتقال إلى المرحلة الثانية من العلاج من قبل لجنة الانتخابات المركزية بناءً على بيانات الفحص السريري والإشعاعي والميكروبيولوجي.
عندما يظهر إفراز البكتيريا (عن طريق الفحص المجهري للبلغم) و/أو في حالة الديناميكيات السريرية والإشعاعية السلبية للعملية بعد شهرين من العلاج، فمن الضروري تحديد حساسية الدواء لمرض السل المتفطرة والتصحيح المناسب للعلاج الكيميائي. أثناء انتظار النتائج، لا يتغير العلاج لمدة شهر واحد. إذا كان من المستحيل اختبار حساسية الدواء، يتم إحالة المريض إلى مؤسسة عليا. يتم تحديد نظام العلاج الإضافي مع الأخذ في الاعتبار حساسية الدواء للعامل الممرض. في الأطفال الذين يعانون من ديناميكيات سريرية وإشعاعية إيجابية بطيئة للعملية، يمكن تمديد المرحلة المكثفة من العلاج لمدة شهر واحد.
مع الديناميكيات السريرية والإشعاعية الإيجابية وغياب المتفطرة السلية وفقًا للفحص المجهري للبلغم، ينتقلون إلى المرحلة الثانية من العلاج - مرحلة الاستمرار.
في مرحلة الاستمراروصف دواءين رئيسيين - أيزونيازيد وريفامبيسين - لمدة 4 أشهر يوميًا أو بشكل متقطع 1 الوضع (3 مرات في الأسبوع). وهناك نظام آخر في مرحلة الاستمرار يمكن أن يكون أيزونيازيد وإيثامبوتول لمدة 6 أشهر.
يمكن أن تستمر عمليات الاسترداد لمدة 8-9 أشهر. يعتبر علاج أورام المعدة الأولية أو المتكررة التي لا يمكن إزالتها جراحيا أكثر فعالية من نقائل سرطان المعدة. إن نقائل سرطان المعدة إلى الكبد والمبيض والغدد الليمفاوية في البطن حساسة للدواء! أصغر - الغدد الليمفاوية في الحوض.
يمكن تحقيق نتائج مرضية في سرطان القولون وخاصة سرطان المستقيم، ولكن فترات التعافي هنا تكون أقصر.
يمكن وصف الفلورويوراسيل بعد الجراحة لمنع الانتكاسات والانتشارات.
طريقة التطبيق. يستخدم فلورويوراسيل عن طريق الوريد، في شكل مرهم 20٪، وكذلك في شكل الحقن داخل الشرايين أو في الوريد والتروية الإقليمية.
وفقا للتعليمات الأمريكية، غالبا ما يستخدم الفلورويوراسيل عن طريق الوريد بمعدل 10-15 ملغ لكل 1 كجم من وزن الجسم. يتم إعطاء الدواء بهذه الجرعة مرة واحدة يوميًا لمدة 4-5 أيام متتالية، إذا لم تتم ملاحظة أي مظاهر سامة، في الأيام التالية يتم إعطاء نصف جرعة من الدواء 4-5 مرات - 7.5 مجم لكل 1 كجم من الجسم. الوزن كل يوم.
عندما تظهر العلامات الأولى للتسمم (التهاب الفم، الإسهال)، يتم إيقاف العلاج. بعد الانتهاء من الدورة، بغض النظر عن وجود أو عدم وجود آثار سامة، لا ينصح بمواصلة العلاج بنفس الدواء. يجب ألا تتجاوز الجرعة اليومية من فلورويوراسيل 1 جرام.
الحالة بعد العلاج الكيميائي
نظرًا لحقيقة أنه بعد استخدام طريقة العلاج هذه بالفلورويوراسيل، غالبًا ما تحدث مضاعفات سامة شديدة، فقد تم تطوير طريقة أكثر لطفًا في معهد الأورام التجريبية والسريرية التابع لأكاديمية العلوم الطبية في اتحاد الجمهوريات الاشتراكية السوفياتية. يتضمن الأخير تناول الفلورويوراسيل كل يومين، مما يجعل من الممكن استخدام جرعة إجمالية أعلى من الدواء وتقليل آثاره الجانبية بشكل كبير.
يتم إعطاء الدواء عن طريق الوريد (بسرعة)، بمعدل 15 ملجم لكل 1 كجم من وزن الجسم يوميًا. الجرعة اليومية هي 0.75-1.5 جرام ويتم الحقن كل يومين. الجرعة الإجمالية لكل دورة علاج هي 3-5 جرام، وفي حالة عدم وجود آثار جانبية - ما يصل إلى 7.5 جرام.
إذا كان المريض يتحمل الدواء جيدًا، فمن المستحسن تكرار مسار العلاج بعد 4-6 أسابيع من أجل إطالة فترة الهدوء. تعتمد الكمية الإجمالية للدواء المستخدم على استجابة المريض لدورة العلاج السابقة. قد يتلقى بعض المرضى ما يصل إلى 5 دورات، وأحيانًا أكثر. مع نظام العلاج هذا، تكون المظاهر السامة خفيفة ويمكن التخلص منها بسهولة.
يتم تحديد عدد الدورات حسب فعالية العلاج وشدة الآثار الجانبية. إذا كان هناك تأثير موضوعي أو ذاتي أو عرضي (تقليل حجم الورم، يتم تحديده عن طريق الجس أو الإشعاعي، تحسن الحالة العامة، اختفاء الألم وأعراض المرض الأخرى)، يتم تكرار دورات العلاج الكيميائي بالفلور راسيل حتى يتم تحقيق هذا التأثير يجب الحفاظ عليها. إذا لم يكن هناك أي تأثير وتقدمت العملية، فمن غير المستحسن وصف الدواء مرة أخرى.
تكرار جلسات العلاج الكيميائي
بعد العلاج بالفلورويوراسيل، يعاني المرضى من انخفاض في حجم الورم، حتى الانحدار الكامل. تستمر فترة الهدأة عادةً من 5 إلى 8 أسابيع، وعدة أشهر، وأحيانًا سنة أو أكثر. بعد الانتهاء من العلاج الكيميائي، استخدم عقار فوتوستيم، خصائصه تمنع ظهور أورام جديدة.
يمكن تحقيق نتائج أفضل عندما يتم الجمع بين العلاج بالفلورويوراسيل والعلاج الإشعاعي، خاصة بالنسبة لسرطان الرئة والمريء والبنكرياس.














