Biblioteca științifică electronică. Histogeneza embrionară. Proliferarea celulară. Creșterea celulară, migrarea și interacțiunile celulă-celulă
PROLIFERARE(din latinescul proles - prole și f it - eu port), termen introdus de Virchow pentru a desemna noua formare a celulelor prin. reproducerea lor prin diviziune. Ca concept general și foarte larg, P. se poate referi la procese de natură foarte diferită. Astfel, celulele P. stau la baza formării țesuturilor regenerative (vezi. Regenerare); P. se observă în diferite hiperplazii (vezi. hiperplazie);în cele din urmă, celulele P. stau la baza creșterii tumorale a țesutului. Desigur, astfel de procese proliferative pot avea loc într-o mare varietate de țesuturi, cu toate acestea, capacitatea elementelor tisulare pentru P. este departe de a fi aceeași: cu cât celulele sunt mai diferențiate, cu atât sunt mai puțin capabile de P.; în special în țesuturi complexe, de exemplu. în epiteliu, P. provine aproape de regulă din acele zone de țesut, care constau din elemente mai puțin diferențiate; Astfel de zone sunt de obicei numite centre de proliferare sau centre de creștere. În epiteliul scuamos multistrat, centrul de proliferare corespunde zonei stratului malpighian sau germinal; în glande, locurile de tranziție ale canalelor excretoare în vezicule glandulare corespund. Consecința P. este de obicei formarea de țesut nou (producția de țesut). totuși, aceasta nu este regula: de exemplu, elementele rezultate din P. inflamator nu formează adesea țesut nou, ci doar pătrund și infiltrează țesutul din jur.
Proliferarea se referă la procesul de diviziune celulară, care duce la o creștere a volumului țesutului. Cea mai activă proliferare are loc în perioada embrionară, când celulele embrionului în curs de dezvoltare se divid continuu și intens. Acest proces este reglat de hormoni și substanțe biologic active care îl pot spori (factorii de creștere) și îl pot slăbi.
Văzând termenul „proliferare” în concluziile experților, mulți încearcă imediat să găsească sensul acestui cuvânt, în același timp se simt îngrijorați de posibilele necazuri, dar nu este nevoie să intre în panică: proliferarea nu este încă o boală.
Celulele multor țesuturi au nevoie de reînnoire constantă; acesta este un proces fiziologic natural realizat prin diviziune. Reînnoirea celulară este deosebit de pronunțată la nivelul pielii și mucoaselor tractului digestiv, sistemul respirator, uter. Adică proliferarea în aceste țesuturi este un fenomen normal și necesar.
Pe de altă parte, proliferarea excesivă a celulelor nu poate fi considerată normală și capătă caracteristici patologice.
Cea mai frecventă manifestare a proliferării este proces inflamator(gastrita, cervicita), leziuni (dupa operatii, traumatisme), tumori. Proliferarea crescută stă la baza proliferării tisulare în neoplasme și procese hiperplazice. Modificările precanceroase, inclusiv displazia, sunt, de asemenea, însoțite de creșterea proliferării celulare.
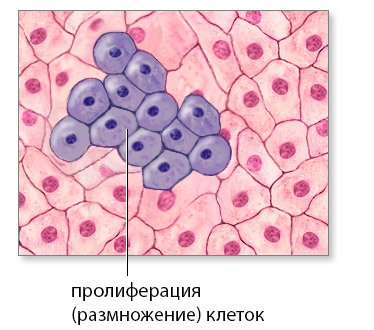 Eu gras modificări inflamatorii sau în leziunile traumatice, proliferarea este, de obicei, de natură tranzitorie și are scopul de a restabili țesutul la normal, dar în cazul tumorilor ea capătă o altă semnificație.În neoplasme, proliferarea nu este doar excesivă, ci și non-stop, celulele se divid continuu, ducând la apariția și creșterea unei tumori. Nu există nicio limită pentru o astfel de proliferare, la fel cum nu există nicio limită pentru diviziunea celulară într-o tumoare.
Eu gras modificări inflamatorii sau în leziunile traumatice, proliferarea este, de obicei, de natură tranzitorie și are scopul de a restabili țesutul la normal, dar în cazul tumorilor ea capătă o altă semnificație.În neoplasme, proliferarea nu este doar excesivă, ci și non-stop, celulele se divid continuu, ducând la apariția și creșterea unei tumori. Nu există nicio limită pentru o astfel de proliferare, la fel cum nu există nicio limită pentru diviziunea celulară într-o tumoare.
Proliferarea este adesea însoțită de atipie, adică celulele în proliferare dobândesc caracteristici neobișnuite pentru ele și se schimbă în aspect și funcționalitate. Atipia indică o posibilă transformare precanceroasă. Apariția unor caracteristici necaracteristice în celule în timpul proliferării crescute nu este surprinzătoare: reproducerea rapidă creează condiții pentru mutatii genetice, iar celulele nu au timp să se maturizeze corespunzător. În acest caz, cantitatea nu înseamnă calitate și, mai devreme sau mai târziu, elemente anormale, mutante, apar într-o clonă de celule care se înmulțește rapid.
Fapt probabilitate mare atipie cu proliferarea celulară face ca acest proces să fie potențial periculos, așa că medicii se feresc de el. Dacă celulele și-au schimbat aspectul sau proprietățile, putem vorbi despre și trebuie să luăm urgent măsuri pentru eliminarea focalizării patologice.
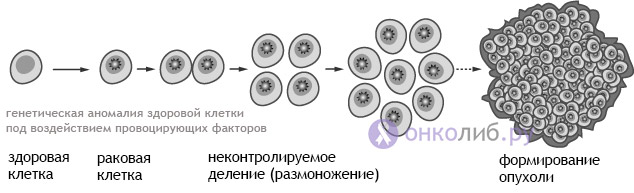
dezvoltarea cancerului - proliferare necontrolată cu atipii
În concluziile morfologilor se poate găsi un indiciu al severității proceselor de proliferare. Acest indicator este destul de subiectiv, deoarece nu există criterii clare pentru a distinge aceste grade. Mai mult, în unele organe, proliferarea moderată poate fi considerată normală, în timp ce în altele, chiar și o ușoară creștere a diviziunii celulare este motiv de îngrijorare. În acest sens, pacienții nu trebuie să se concentreze prea mult pe grad, dar dacă vorbim de proliferare patologică, atunci este clar că cu cât este mai puternic, cu atât mai rău.
Video: despre diviziunea celulară și dezvoltarea cancerului
Proliferare în ginecologie (endometru și col uterin)
Poate că obstetricienii și ginecologii se confruntă cel mai adesea cu fenomenul de proliferare. Diviziunea celulară în organele genitale feminine are loc foarte activ în mod normal și chiar mai intens în patologie. Prezența proliferării este menționată în concluzie examen histologic membrana mucoasă a corpului uterin sau a canalului cervical, un fragment de col uterin îndepărtat prin conizare.

Pe baza concluziei, medicul ginecolog trage concluzii despre normă sau patologie, iar femeia care primește rezultatul în mâinile ei caută să afle mai multe despre esența proliferării. Nu este un secret pentru nimeni că mulți specialiști nu sunt foarte vorbăreți și nu se răsfăț explicatii detaliate semnificația termenilor individuali, așa că să încercăm să ne dăm seama ce ar putea însemna proliferarea în uter și ce să facem în acest sens.
Uterul în diferite departamente are o structură diferită și căptușeală diferită. Astfel, partea exterioară a colului uterin este acoperită cu epiteliu scuamos multistrat, canalul cervical este căptușit cu cilindric, iar membrana mucoasă a corpului organului (endometrul) este un țesut glandular complex. Pentru ciclu menstrual uterul suferă fluctuații ale hormonilor sexuali și se pregătește pentru o potențială sarcină, astfel că proliferarea este nu numai normală, ci și un mecanism vital care asigură modificări ale endometrului pentru o implantare confortabilă.
Proliferarea epiteliului scuamos stratificat al colului uterin exterior are sens numai pentru a reînnoi stratul tegumentar, prin urmare În mod normal, nu ar trebui să fie prea pronunțat. La femeile însărcinate, din cauza modificărilor hormonale, este detectată o proliferare moderată a epiteliului glandular al colului uterin, ceea ce nu este considerat o patologie.
Creșterea proliferării epiteliale poate indica:
- proces inflamator (cervicita);
- Leziuni traumatice ( chiuretaj de diagnostic, avorturi, îndepărtarea fragmentelor de col uterin alterate patologic, rupturi în timpul nașterii);
- Creșterea tumorii (papiloame, displazie).
Astfel, pe baza factor cauzal, condiționat, proliferarea este izolată în colul uterin inflamator(cervicita), hiperplazic(polipi, pseudoeroziuni, tumori) și post-traumatic(lacrimi, modificări de cicatrice).
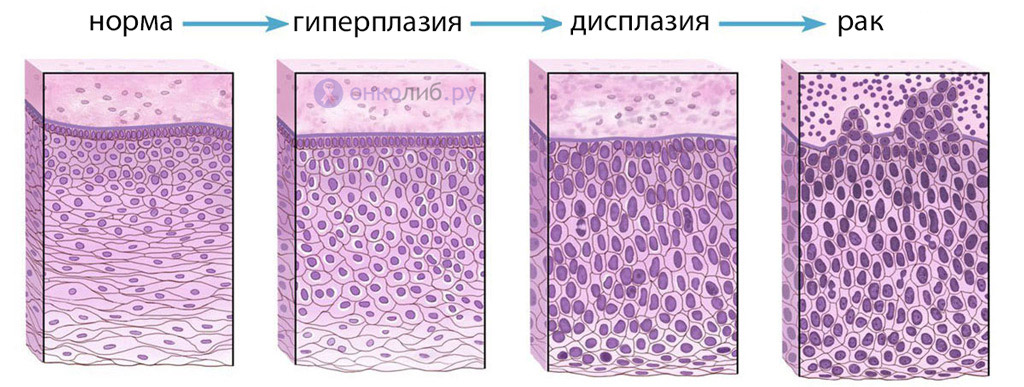
transformarea țesutului sănătos în țesut tumoral
Diverse tipuri de cervicite (bacteriene, virale, fungice) duc inevitabil la deteriorarea epiteliului tegumentar, care, în efortul de a-și restabili integritatea, începe să prolifereze activ. Pe acest fond, se exprimă și alte semne de inflamație - infiltrarea de către celulele inflamatorii (leucocite, limfocite, macrofage), vasodilatație microvasculară, umflare, astfel încât cauza creșterii proliferării celulare este de obicei clară.
Schimbări similare apar cu eroziunea adevărată, afectarea colului uterin în timpul nașterii, avortul și manipularea intrauterină. Proliferarea reflectă regenerarea (restaurarea) epiteliului scuamos stratificat și este mai degrabă fiziologică.
Diviziunea celulară accelerată cu modificările de mai sus nu este de obicei periculoasă, deși necesită tratament cu monitorizarea ulterioară a eficacității sale. Dacă membrana mucoasă și-a revenit, atunci nu există niciun motiv de îngrijorare.
Proliferarea epiteliului cu atipie. În plat multistrat acoperă epiteliul atipia însoțește adesea deteriorarea de către tipurile oncogene de papilomavirus, când riscul de transformare malignă este foarte mare, precum și pseudo-eroziunea colului uterin, denumită în mod popular pur și simplu eroziune.
Pseudo-eroziunea este apariția în partea exterioară a colului uterin a epiteliului glandular, similar cu cel care căptușește în mod normal canalul cervical. Procesul este dezhormonal în natură și are loc adesea pe fundal infectie viralași cervicita. Proliferarea în pseudoeroziuni se referă atât la epiteliul plat, care crește în aceste focare, încercând să le „neutralice”, cât și la epiteliul cilindric, care formează glandele erozive în sine.
Proliferarea excesivă a epiteliului glandular în structurile de pseudoeroziuni duce la formarea de papile, ramuri și noi glande în grosimea colului uterin. Proliferarea celulelor epiteliale scuamoase, care caută să înlocuiască complexe glandulare anormale, este adesea însoțită de displazie, ceea ce înseamnă că procesul a luat calea formării cancerului.
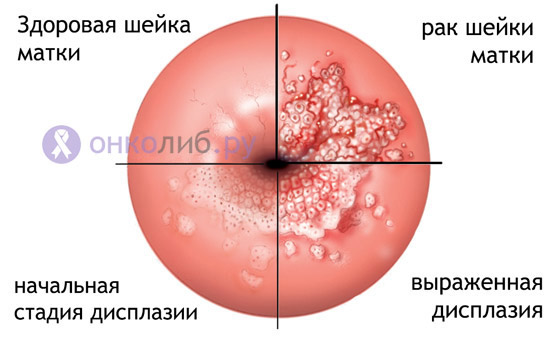 Proliferarea cu displazie în epiteliul scuamos stratificat este cea mai periculoasă combinație. Creșterea proliferării celulelor, perturbarea orientării lor corecte în grosimea stratului epitelial, apariția unor caracteristici externe anormale - toate acestea sunt semne de displazie, principalul proces precanceros al colului uterin.
Proliferarea cu displazie în epiteliul scuamos stratificat este cea mai periculoasă combinație. Creșterea proliferării celulelor, perturbarea orientării lor corecte în grosimea stratului epitelial, apariția unor caracteristici externe anormale - toate acestea sunt semne de displazie, principalul proces precanceros al colului uterin.
Canalul cervical care duce în uter este căptușit cu epiteliu columnar, care este, de asemenea, destul de capabil de reproducere. În mod normal, proliferarea epiteliului columnar este necesară pentru reînnoirea celulară, dar apare și în patologie - inflamație, polipi ai canalului cervical, adenoame, carcinoame.
Endometrul este stratul interior al corpului uterin, care are organizare complexăși își schimbă continuu structura pe tot parcursul ciclului menstrual. În timpul fazei de descuamare (sângerare), este respins dacă sarcina nu a avut loc, apoi trebuie să se formeze din nou și să crească în volum. Acest lucru se întâmplă tot timpul. Este clar că acest lucru nu se poate face fără proliferare; celulele trebuie să se dividă activ, restabilind endometrul care a fost descuamat în timpul menstruației.
Proliferarea celulelor endometriale are loc cel mai activ în prima jumătate a ciclului, care se numește faza de proliferare. În această perioadă, mucoasa uterină se află sub influența estrogenilor, produși activ în ovar, în timp ce următorul ovul se maturizează acolo.
Proliferarea se referă în mare măsură la glandele endometriale, care trebuie să se „alungească” cât mai mult posibil înainte de ovulație. În proliferarea timpurie (5-7 zile ale ciclului), glandele sunt reprezentate de tuburi înguste cu nuclee de culoare închisă, dar la 8-10 zile (etapa de mijloc a fazei de proliferare) încep să capete un aspect contorsionat, există numeroase mitoze, ceea ce indică diviziunea celulară activă. Până în a 14-a zi a ciclului menstrual, există multe glande, sunt întortocheate, nucleii celulari sunt la diferite niveluri. În acest moment, proliferarea trebuie să cedeze faza următoare – secreția. Acest lucru se întâmplă în mod normal.
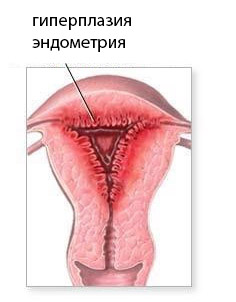 În patologie, proliferarea pronunțată a componentelor endometriale reflectă procese hiperplazice și tumori. Hiperplazia endometrială nu este altceva decât proliferare, care nu s-a oprit în timp, trecând în faza secretorie de maturare a membranei mucoase. Proliferarea crescută a celulelor endometriale duce la apariția unei componente glandulare în exces, transformare chistică și este plină de atipii.
În patologie, proliferarea pronunțată a componentelor endometriale reflectă procese hiperplazice și tumori. Hiperplazia endometrială nu este altceva decât proliferare, care nu s-a oprit în timp, trecând în faza secretorie de maturare a membranei mucoase. Proliferarea crescută a celulelor endometriale duce la apariția unei componente glandulare în exces, transformare chistică și este plină de atipii.
Există hiperplazie endometrială difuză, când întreaga mucoasă uterină este îngroșată și nu corespunde fazei ciclului, și polipi endometriali focali. Polipii pot fi proliferativi, când simptomul principal este diviziunea epiteliului glandular, și secretori, mai caracteristici fazei a doua a ciclului.
Punctul cheie în evaluarea clinică a hiperplaziei endometriale este prezența sau absența atipiei (hiperplazie atipică sau neatipică). Celulele care se divid rapid sub influența hormonilor devin mai susceptibile de a suferi mutații, astfel încât atipia este o consecință probabilă a proliferării și hiperplaziei.
Pentru hiperplazia glandulară neatipică, țesutul afectat este îndepărtat, iar medicul ginecolog decide asupra terapiei conservatoare suplimentare. Hiperplazia atipică poate necesita măsuri mai radicale până la histerectomie, deși astfel de decizii sunt luate ținând cont de vârsta, cauzele hiperplaziei și planurile de reproducere ale femeii.
Astfel, proliferarea în uter nu are o semnificație independentă ca patologie, aceasta nu este o boală ca atare, ea reflectă doar procesele care au loc acolo și poate fi o consecință atât a normalității, cât și a patologiei. Atitudinea față de proliferarea în uter este determinată de cauzele și localizarea acesteia:
- În colul uterin fără atipie pe fondul inflamației, traumatismelor, eroziunii - tratament conservator;
- În colul uterin cu atipie - îndepărtarea zonei afectate, tratament conservator în funcție de cauză (hormoni, antimicrobiene etc.);
- În endometru, proliferarea în prima jumătate a ciclului este normală, nu există motive de îngrijorare la pacient vârsta reproductivă, în menopauză, orice proliferare indică reluarea creșterii endometrului și necesită o examinare atentă (hiperplazie, polip, cancer sunt posibile);
- Proliferarea cu hiperplazie este un fenomen periculos care necesită chiuretajul cavității uterine și terapie hormonală;
- Proliferarea cu atipie este o afecțiune precanceroasă care implică îndepărtarea întregului endometru sau a uterului.
Proliferarea tumorii înseamnă o creștere a volumului țesutului tumoral prin divizarea celulelor acestuia, adesea cu atipie. Nu are o semnificație independentă, ci caracterizează doar creșterea neoplaziei, adică dacă există o tumoare, va exista o proliferare, iar cât de repede va crește neoplazia depinde de severitatea acesteia. carcinoame cervicale, canalul cervicalși sunt întotdeauna însoțite de o proliferare crescută, care este vizibilă deja în stadiul de displazie.
Proliferare în gastroenterologie
Proliferarea epiteliului gastric are loc normal și continuu. Membrana mucoasă a acestui organ are nevoie de reînnoire regulată, astfel încât celulele se împart activ. În același timp, orice deteriorare provoacă o accelerare a diviziunii celulare.
Principalele motive care determină creșterea proliferării epiteliului gastric sunt gastrita, ulcerele, polipii și tumorile. La acut gastrită pe fondul unei componente inflamatorii pronunțate sub formă de umflare a membranei mucoase, descuamare a stratului de suprafață, hemoragii, zone de proliferare epiteliul gropii tegumentale, care reflectă procesul de regenerare a membranei mucoase.
Gastrita cronică, atât de comun în toate zilele astea grupe de vârstă, apar și cu proliferarea crescută a epiteliului. Acest proces este evident mai ales când forme hiperplazice boli când membrana mucoasă se îngroașă, sunt posibile creșteri polipoide.
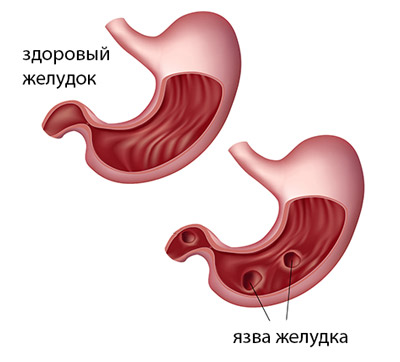 Ulcer la stomacîn timpul exacerbării, apare cu afectarea peretelui organului, pe care organismul încearcă să-l elimine. Rezultatul este proliferarea epiteliului, exprimată clar în margini defect ulcerativ. Această proliferare este asociată polipi hiperplazici, des întâlnit la marginile ulcerului.
Ulcer la stomacîn timpul exacerbării, apare cu afectarea peretelui organului, pe care organismul încearcă să-l elimine. Rezultatul este proliferarea epiteliului, exprimată clar în margini defect ulcerativ. Această proliferare este asociată polipi hiperplazici, des întâlnit la marginile ulcerului.
Un pericol deosebit este proliferarea precanceroasă în peretele stomacului când celulele întunecate alungite de la gâturile glandelor gastrice încep să se înmulțească. Inițial, acest proces este de natură regenerativă, dar deoarece diferențierea celulară este afectată, recuperare normală mucozizarea nu are loc. În schimb, glandele sunt acoperite cu celule cu nuclee întunecate, alungite, situate la baza lor.
Proliferarea precanceroasă poate fi limitată sau difuză, dar se găsește întotdeauna în secțiunile superioare glandele, în timp ce straturile mai profunde rămân puțin modificate. Celulele întunecate ale epiteliului displazic nu secretă mucus și, în consecință, nu își îndeplinesc funcțiile directe. De-a lungul timpului, acestea înlocuiesc căptușeala glandulare normală, înlocuindu-l complet.
Următoarea etapă a unei astfel de proliferări este dezvoltarea, iar aceasta poate fi o zonă mică a unei glande. Transformarea malignă are loc în orice moment, dar pe fondul proliferării precanceroase existente și al structurii normale a altor glande.
Sânul

Modificările sânilor sunt destul de frecvente, inclusiv în rândul fetelor și femeilor tinere. Organul experimentează în mod constant acțiunea hormonilor sexuali și suferă modificări caracteristice pe tot parcursul ciclului menstrual, în timpul sarcinii și alăptării, deci sensibile diferite feluri patologie. Conform statisticilor, până la 60% dintre femeile de vârstă reproductivă prezintă semne de mastopatie.
Mastopatia este considerată un proces benign, dar dacă este prezentă, riscul de malignitate crește de câteva ori. Variantele proliferative sunt și mai periculoase, cresc probabilitatea de cancer de 25-30 de ori.
Prezența sau absența proliferării este cel mai important semn în evaluarea tipului de mastopatie. Forme neproliferative reprezentate prin focare țesut fibros, canale alterate chistic, al căror epiteliu nu proliferează și este chiar atrofic. Riscul de transformare malignă este relativ mic.
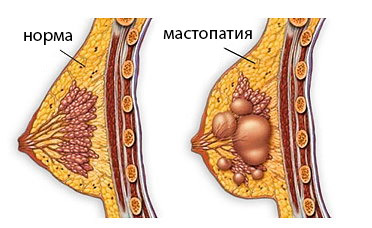 Mastopatie proliferativă mult mai periculos, deoarece celulele conductelor și lobulilor glandei se divid activ, creând amenințarea degenerării canceroase. Cu cât mai multe astfel de focare de proliferare în țesutul glandei și cu cât proliferarea componentei epiteliale este mai activă, cu atât este mai probabilă în viitor, prin urmare toate formele de mastopatie proliferativă sunt considerate afecțiuni precanceroase.
Mastopatie proliferativă mult mai periculos, deoarece celulele conductelor și lobulilor glandei se divid activ, creând amenințarea degenerării canceroase. Cu cât mai multe astfel de focare de proliferare în țesutul glandei și cu cât proliferarea componentei epiteliale este mai activă, cu atât este mai probabilă în viitor, prin urmare toate formele de mastopatie proliferativă sunt considerate afecțiuni precanceroase.
În funcție de severitatea proliferării, se disting mai multe grade de mastopatie. În primul grad, proliferarea nu este detectată, în al doilea, este acolo, dar celulele nu prezintă semne de atipie, al treilea grad de mastopatie se manifestă prin proliferarea activă a celulelor epiteliale cu atipie.
Astfel, proliferarea celulelor glandei mamare nu este doar un criteriu pentru forma de mastopatie, ci și un indicator al probabilității de cancer, prin urmare diviziunea excesivă a epiteliului atrage întotdeauna atenția specialiștilor. Diagnosticul acestei modificări se realizează prin examinarea citologică a țesutului obținut în timpul puncției.
Ce să faci dacă există proliferare?
Dacă proliferarea este detectată oriunde, specialistul va determina mai întâi cauza acesteia și apoi va întocmi un plan de management pentru pacient. Nu există un tratament specific pentru proliferare ca atare, deoarece nu este o patologie independentă, ci o reflectare a altor boli. Dacă creșterea diviziunii este cauzată de inflamație, medicul va prescrie terapie antiinflamatoare, suplimentând-o cu agenți antibacterieni sau antivirali, dacă este necesar.
Proliferarea precanceroasă cu atipie pe fondul displaziei poate necesita măsuri mai radicale - excizia zonei afectate.În cazul proliferării pe fundal, tratamentul se efectuează conform tuturor principiilor îngrijirea cancerului până la prelevarea organului.
Orice proliferare care indică patologie servește ca un semnal alarmant, astfel încât pacienții cu astfel de modificări sunt întotdeauna în câmpul vizual al medicului. După tratamentul bolii de bază, de obicei se efectuează un test de control. examen citologic sau biopsie, permițând evaluarea eficacității terapiei și a riscului de transformare a tumorii în viitor.
Masele celulare care alcătuiesc nodulul (notate prin termenul „granulema”) constau din celule limfoide, epitelioide, plasmatice, adesea cu un amestec de celule gigantice cu numeroși nuclei. Compoziția citologică a granuloamelor variază datorită raporturilor cantitative diferite ale acestor elemente. Astfel, în părțile centrale ale granuloamelor tuberculoase - tuberculi, se observă acumulări de celule epitelioide ușoare și, de asemenea, celule gigantice, iar la periferie există o zonă de celule limfoide. Celulele plasmatice sunt adesea împrăștiate difuz în jurul acestor granuloame; acestea din urmă pot predomina în general brusc, formând infiltrate continue. Pentru celulele gigantice din tuberculii tuberculoși, este tipic un aranjament periferic al nucleelor, formând un fel de inel sau semi-inel (celule Pirogov-Langhans).
Granuloamele se observă, de asemenea, în sifilis, lepră, bruceloză, febră tifoidă, reumatism, rinosclerom, mucă, encefalita virala, rickettzioze, de exemplu, tifos, cu diferite infecții fungice (actinomicoză, aspergiloză, blastomicoză etc.).
În sifilis, granuloamele (gumele) constau în principal din celule limfoide și plasmatice. De obicei vorbim despre fuzionarea infiltratelor, formând noduri mari până la ou de gainași altele. Caracterizat printr-o abundență de vase în părțile periferice ale gumei și procese productive din partea intimei vaselor, ceea ce duce adesea la obliterarea acestora. Împreună cu gumele clar definite, în sifilis se formează infiltrate gingivale difuze, de exemplu, în meningele moi.
În lepră, granuloamele (leproamele) și infiltratele difuze se caracterizează printr-un conținut abundent de bacili de lepră. Bacilii sunt localizați în protoplasma unor „celule de lepră” mari, numite uneori „bile” din cauza formei rotunjite a acestor macrofage deosebite („celule Virchow”).
Cu bruceloză, împreună cu granuloamele miliare * tipice, care în compoziția lor celulară seamănă cu tuberculii tuberculoși, infiltratele difuze sunt și mai des observate, de exemplu, în meningele moi ale creierului și măduvei spinării.
În febra tifoidă, sub formă abdominală de paratifoid, granuloamele care apar în sistemul limfatic al intestinului (foliculi solitari, plasturi Peyer), în ficat, splină, uneori în laringe, căile biliare, au structura unor noduli vagi de celule reticulare mari („celule tifoide". În reumatism, granuloamele se formează, de regulă, în țesuturile dense, de exemplu, în straturile fibroase ale miocardului, în valvele cardiace, fascia, aponevroze, țesuturi paraarticulare. Aceasta a servit ca bază pentru clasificarea reumatismului acut drept „colagenoză”, adică boli care se bazează pe anumite forme de dezorganizare a colagenului, care provoacă o reacție celulară productivă.
Granuloamele reumatice sunt uneori submicroscopice, uneori sunt noduli și noduri de dimensiunea unui bob de orez până la o nucă. Se caracterizează prin proliferarea macrofagelor mari (în special în miocard), precum și a limfocitelor, fibroblastelor sub formă de rozete și palisade. În rinosclerom, granuloamele sunt reprezentate în principal de celule plasmatice și epitelioide. „Celulele Mikulich” mari sunt specifice, conținând un număr mare de tije de rinosclerom, precum și „bile hialine” deosebite, care sunt un produs al transformării citoplasmei celulelor plasmatice. Procesul este cel mai adesea localizat în membrana mucoasă a nasului, faringelui și laringelui și duce la o îngustare a lumenului acestora.
La morva, granulomatoza, sau mai degrabă procesele de granulare-purulente, se observă în primul rând în tractul respirator (nas, plămâni), precum și în piele. Granuloamele constau din celule epitelioide și leucocite. Caracterizat prin dezintegrarea celulelor de granulom și infiltrate difuze cu formarea de câmpuri extinse de cariorexis. Tranzițiile în supurația vulgară sunt frecvente; puroiul este deosebit de vâscos.
Modificări similare apar într-o boală asemănătoare morvei cunoscută sub numele de melioidoză (o boală a țărilor tropicale). În encefalita virală, granuloamele se dezvoltă în principal în materie cenusie sistem nervos central; sunt formate în principal din celule microgliale. Granuloamele din tifos arată similar.
Granuloamele din bolile fungice sunt fie clar definite, fie au aspectul unor infiltrate difuze care conțin celule plasmatice, epiteliale, gigantice și ciuperci corespunzătoare sub formă de fire împletite sau colonii în formă de stea - Drusen, vizibile cu ochiul liber, de exemplu, cu akt despre micoză. Este important din punct de vedere diagnostic ca în aproape 50% din cazuri drusele să fie absente, suferind liză, calcificare, absorbție de către celule gigantice sau transformare într-o masă sticloasă (A. V. Talalaeva și D. I. Asnin, 1964). În mod caracteristic, pe fondul sclerozei lemnoase extinse, există focare împrăștiate de supurație, adesea tracturi fistuloase și formarea de focare de celule xantom în țesutul cicatricial.
Dinamica procesului granulomatos se încadrează în următoarele patru faze:
alterarea primară a țesutului;
dezvoltarea granulomului celular;
distrugerea celulelor granulomului;
scleroza reziduală sau încapsularea leziunii.
Cu alterarea primară, vorbim de modificări degenerative și necrobiotice ale endoteliului vascular, viitorul centru al granulomului. Aceste modificări se datorează absorbției de către endoteliu a anumitor agenți biologici și biochimici care au proprietăți antigenice și capacitatea de a provoca un răspuns adecvat. Astfel de agenți pot fi microorganisme care circulă în sânge sau limfă, toxinele acestora, proteinele corporale denaturate, corpuri străine, a intrat accidental în corp.
Alterarea primară a țesutului este adesea asociată cu tromboza vaselor. Adesea, conexiunile cu vasul nu pot fi detectate și vorbim despre „dezorganizarea” primară (V.T. Talalaev, 1929) a stromei, în special a fibrelor de colagen, așa cum se întâmplă, de exemplu, în reumatismul acut. Centrul unui viitor granulom poate fi celule ganglionare care au suferit distrugeri, așa cum se observă în encefalita virală.
A doua fază a dezvoltării granulomului din punct de vedere morfologic și histogenetic este mai mult stereotipă decât strict specifică în raport cu, de exemplu, diverse infecții. Într-adevăr, granuloamele conțin în esență aceleași celule în proporții diferite. Acest lucru este de înțeles, deoarece materialul celular folosit pentru a construi granuloamele are aproape întotdeauna o singură sursă, și anume endoteliul, celulele adventițiale și alte celule de origine mezenchimală. Celulele gliale joacă un rol activ în construcția granuloamelor în sistemul nervos și a celulelor mezoteliale din cavitățile corpului. Asemănarea citologică a granuloamelor în diferite boli infecțioase se explică și prin faptul că baza biologică a granulomatozei, și anume imunogeneza, este similară.
Citologic, granuloamele pot fi construite cu o oarecare originalitate. Deci, în unele există multe celule gigantice, în altele nu există deloc, în unele predomină puternic celulele epitelioide, iar în altele - limfoide, plasmatice etc. Acest lucru vă permite să navigați practic în recunoașterea naturii bolii.
Cu toate acestea, această unicitate este asociată nu numai cu caracteristicile agentului, de exemplu, o infecție, ci și cu caracteristicile organismului, ca să nu mai vorbim de specificul substratului, de exemplu. locul de dezvoltare a granulomului. Cu alte cuvinte, trei cantități determină granulomatoza și expresia ei morfologică specifică, iar fiecare dintre aceste cantități (agent, organism, țesut sau organ) are întotdeauna o anumită gamă de labilitate.
Stimulul imediat pentru granulomatoză sunt substanțele chimice care apar în timpul procesului de alterare primară. Acestea pot fi produse ale denaturarii țesuturilor, în special substanțe cu proprietățile autoadlergenilor, produse reziduale ale microorganismelor, precum și produse ale degradarii acestora. Granuloamele tipice de tuberculoză pot fi obținute prin introducerea de bacili de tuberculoză morți (Koch, 1884; V.K. Vysokovich, 1890) și chiar de substanțe chimice obținute în timpul prelucrării lor (ceară, fosfatide etc.). Aceste substanțe chimice sunt adesea împărtășite de diferiți microbi. De aceea tuberculii tipici de tuberculoză cu celule gigantice și necroză brânză pot fi obținuți prin introducerea de fosfatide extrase din bacilii de iarbă de timothy din bacilii de lepră.
A treia fază - distrugerea celulelor granulomului - se exprimă fie în necroza centrului granulomului (necroză brânză în tuberculoză, carie gingioasă în sifilis), fie în degenerarea treptat progresivă a celulelor sale, imperceptibilă pe fondul transformării granulomul într-un focar de scleroză. Distrugerea poate dobândi caracteristici ale necrozei de lichefiere, adică. lichefiere, iar uneori semne de supurație (mucară, tuberculoză, infecții fungice). ÎN acest din urmă caz scleroza terminală este deosebit de extinsă.
Semnificația clinică a granulomatozei este adesea determinată tocmai de scleroză (faza a patra), localizarea acestora și suprafața totală. Scleroza reumatică, care apare de-a lungul sistemului de conducere al inimii, implică tulburări în conducerea excitației pe drumul de la nodul sinusal către camerele inimii, până la așa-numitul bloc cardiac. Granulomatoza cu leziuni sifilitice ale aortei, însoțită de colapsul structurilor elastice, stă la baza dilatațiilor anevrismale ale aortei. Diverse deformări de organ sub formă de ficat lobulat, plămân (hepar lobatum, pulmo lobatum), picioare în formă de sabie, retragerea punții nazale, obliterarea lumenelor vaselor de sânge etc. caracterizează granulomatoza sifilitică a localizării corespunzătoare.
Tulburările metabolismului proteic sub formă de amiloidoză sunt adesea o consecință a formelor recurente de granulomatoză în tuberculoză, actinomicoză, mai ales atunci când aceste infecții sunt combinate cu carii extinse și supurație. Pierderea completă a funcției suprarenale în boala Addison se bazează de obicei pe granulomatoza tuberculoasă difuză. Relativ acută în cursul său este granulomatoza virală și rickettsială a sistemului nervos central, care nu poate lăsa în urmă consecințe nu numai clinice, ci chiar anatomice (de exemplu, tifos). Mai des, însă, întregul ciclu de dezvoltare al granuloamelor acoperă perioade semnificative, de exemplu, o lună sau mai mult și efecte reziduale, adică scleroza poate fi vizibilă. Acest lucru aduce inflamația proliferativă mai aproape de formele sale cronice, unde fiecare ciclu se termină cu formarea unei cicatrici.
O altă proprietate a formelor proliferative de inflamație este tendința lor de a recidiva după vindecare luni de zile, uneori ani și decenii mai târziu (bruceloză, tuberculoză, reumatism, sifilis etc.).
Întrebarea motivelor pentru care procesele inflamatorii preiau caracteristicile granulomatozei, care este combinată cu o extindere a cursului bolii, care adesea capătă o natură cronică, este rezolvată de patologia modernă dintr-o poziție imunologică.
Cu alte cuvinte, granulomatoza nu este o proprietate unilaterală sau specifică a infecției, de exemplu. microbi patogen. Granulomatoza ar trebui considerată ca o expresie morfologică a unei relații imunologice unice între „gazdă” și „oaspete”, adică. între corp și infecție. Prin urmare, granulomatoza reflectă dinamica procesului de imunizare, etapele și variațiile cantitative ale acestuia.
Cât de mari sunt variațiile cantitative este dovedit de cazurile de tuberculoză miliară (adică formarea unui număr nenumărat de granuloame minuscule), pe de o parte, și cazurile de granuloame unice, detectate accidental, pe de altă parte.
Leishmania (Leishmania tropica), clasa de protozoare. Sunt agenți cauzali ai leishmaniozei cutanate, numite Pendinsky, sau ulcerului oriental, precum și leziuni viscerale (kalaazar). Un proces cutanat are loc la locul mușcăturii de insectă (flebotom), mai întâi sub formă de nodul, care apoi se ulcerează. De obicei, formarea de granuloame multiple din celulele epitelioide care conțin Leishmania.
F i l i r i (Filaria Bancrofti), clasa de nematozi. Sunt agenți cauzali ai filariozei; transmisă de țânțari. Procesul este localizat în piele de-a lungul sistemului limfatic și este cronic; însoțită de hiperproducție de țesut conjunctiv, așa-numita elefantiază a extremităților inferioare, răspândirea scrotului în țesutul retroperitoneal, limfangita cronică și limfadenita.
Finlandezul teniei echinococice (Taenia echinococcus), care parazitează intestinele câinilor, este denumit echinococcus, care poate fi cu o singură cameră sau cu mai multe camere și de dimensiunea unei nuci de pin până la capul unui adult. Procesele productive sunt deosebit de extinse în echinococul multilocular al ficatului.
Același tip de simbioză areactivă se observă în sistemul nervos central în unele spirochetoze, de exemplu, în paralizia progresivă și febra recidivante.
În dezvoltarea inferioarelor şi vertebrate superioare un singur model biologic general este clar vizibil, exprimat în aspectul straturilor germinale și separarea principalelor rudimente ale organelor și țesuturilor. Procesul de formare a țesuturilor din materialul rudimentelor embrionare este esența doctrinei histogenezei.
Histogeneza embrionară, așa cum este definit de A.A. Klishova (1984) este un complex de procese de proliferare, creștere celulară, migrare, interacțiuni intercelulare, diferențiere, determinare, moarte celulară programată și altele, coordonate în timp și spațiu. Toate aceste procese, într-o măsură sau alta, au loc în embrion, începând chiar de la început primele etape dezvoltarea acestuia.
Proliferare. Principalul mod în care celulele tisulare se divid este mitoza. Pe măsură ce numărul de celule crește, apar grupuri sau populații de celule, unite printr-o locație comună în straturile germinale (rudimente embrionare) și care posedă potențe histogenetice similare. Ciclul celular este reglat de numeroase mecanisme extracelulare și intracelulare. Influențele extracelulare asupra celulei includ citokine, factori de creștere, stimuli hormonali și neurogeni. Rolul regulatorilor intracelulari este jucat de proteinele citoplasmatice specifice. În timpul fiecărui ciclu celular, există mai multe puncte critice care corespund tranziției celulei de la o perioadă a ciclului la alta. În caz de încălcare sistem intern control, celula, sub influența propriilor factori de reglare, este eliminată prin apoptoză, sau este întârziată ceva timp într-una din perioadele ciclului.
Metoda analizei radiografice ciclurile celulare din diferite țesuturi au relevat particularitățile relației dintre reproducerea și diferențierea celulelor. De exemplu, dacă țesuturile (țesuturile hematopoietice, epiderma) au un fond constant de celule în proliferare, care asigură apariția continuă a celulelor noi care să le înlocuiască pe cele muribunde, atunci aceste țesuturi sunt clasificate ca reînnoitoare. Alte țesuturi, de exemplu, unele țesuturi conjunctive, se caracterizează prin faptul că în ele are loc o creștere a numărului de celule în paralel cu diferențierea lor; celulele din aceste țesuturi se caracterizează printr-o activitate mitotică scăzută. Acestea sunt țesuturi în creștere. In cele din urma, țesut nervos caracterizată prin faptul că toate procesele principale de reproducere se termină în perioada histogenezei embrionare (când se formează sursa principală de celule stem, suficientă pentru dezvoltarea ulterioară a țesuturilor). Prin urmare, este clasificat ca țesut stabil (staționar). Durata de viață a celulelor în țesuturile reînnoite, în creștere și stabile este diferită.
Odată cu reînnoirea celulară populatiilor, în celulele înseși, se observă constant reînnoirea structurilor intracelulare (regenerare fiziologică intracelulară).
Creșterea celulară, migrarea și interacțiunile celulă-celulă. Creșterea celulară se manifestă prin modificări ale dimensiunii și formei lor. Cu activitate funcțională crescută și biosinteză intracelulară, se observă o creștere a volumului celular. Dacă volumul celular depășește o anumită normă, atunci vorbim de hipertrofia acestuia, și invers, cu scăderea activității funcționale, volumul celular scade, iar când se depășesc anumiți parametri normativi se produce atrofia celulară. Creșterea celulară nu este nelimitată și este determinată de raportul optim nuclear-citoplasmatic.
Procesele de mișcare sunt importante pentru histogeneză celule. Migrarea celulară este cea mai tipică în timpul perioadei de gastrulație. Cu toate acestea, chiar și în perioada histo- și organogenezei, au loc mișcări ale maselor celulare (de exemplu, deplasarea mioblastelor din miotomi la locurile de formare a mușchilor scheletici; mișcarea celulelor din creasta neură cu formarea ganglionilor spinali și a nervilor. plexuri, migrarea gonocitelor etc.). Migrația se realizează folosind mai multe mecanisme. Astfel, se face o distincție între chemotaxia - mișcarea celulelor în direcția unui gradient de concentrație a unui agent chimic (mișcarea spermatozoizilor către ovul, precursori ai limfocitelor T din măduvă osoasă la mucoasa timusului).
Haptotaxie- mecanism de mișcare a celulelor de-a lungul gradientului de concentrație al moleculei de adeziune (deplasarea celulelor ductului pronefros la amfibieni de-a lungul gradientului de fosfatază alcalină pe suprafața mezodermului). Orientare de contact - atunci când în orice obstacol rămâne doar un canal pentru mișcare (descris la pești în timpul formării aripioarelor).
Inhibarea contactului- aceasta metoda de miscare este observata in celulele crestei neurale. Esența metodei este că atunci când o lamelipodie este formată de o celulă și intră în contact cu o altă celulă, lamelipodia se oprește din creștere și dispare treptat, dar se formează o nouă lamelipodie într-o altă parte a celulei migratoare.
În curs migrație celulelor, interacțiunile intercelulare joacă un rol important. Există mai multe mecanisme ale unei astfel de interacțiuni (de contact și la distanță). Este identificat un grup mare de molecule de adeziune celulară (MCA). Astfel, caderinele sunt mAb dependenți de Ca2+, responsabili de contactele intercelulare în timpul formării țesuturilor, de formarea formei etc. Molecula de caderină distinge între domeniile extracelular, transmembranar și intracelular. De exemplu, domeniul extracelular este responsabil pentru aderența celulelor cu aceleași cadherine, iar domeniul intracelular este responsabil pentru forma celulei. O altă clasă de mAb este superfamilia de imunoglobuline a mAb-urilor independente de Ca2+, care asigură, de exemplu, aderența axonilor la sarcolemă. fibre musculare, sau migrarea neuroblastelor de-a lungul gliocitelor radiale din cortexul cerebral etc. Următoarea clasă de mCA este enzimele membranare - glicoziltransferaze. Acestea din urmă, ca o „blocare cu cheie”, se conectează cu substraturi de carbohidrați - glicozaminoglicanii complexului supramembranar al celulei, asigurând astfel o aderență puternică a celulelor.
Cu exceptia mecanisme de interacțiune intercelulară, există mecanisme de interacțiune a celulelor cu substratul. Acestea includ formarea de receptori celulari pentru moleculele matricei extracelulare. Acestea din urmă includ derivați celulari, printre care moleculele de adeziune cele mai studiate sunt colagenul, fibronectina, laminina, tenascina și altele. Colagenii, printre care există câteva zeci de tipuri, fac parte din substanța intercelulară a țesutului fibros lax. țesut conjunctiv, membrana bazală etc. Fibronectina, secretată de celule, este o moleculă de legare între celula migratoare și matricea extracelulară. Laminina, o componentă a membranei bazale, conectează, de asemenea, celulele migratoare cu matricea intercelulară (adevărat pentru celulele epiteliale și neuroblaste).
A implementa comunicarea dintre celulele migratoare celulele formează receptori specifici cu matricea intercelulară. Acestea includ, de exemplu, sindecanul, care asigură contactul celulei epiteliale cu membrana bazală datorită aderenței la moleculele de fibronectină și colagen. Integrinele de suprafață celulară leagă moleculele matricei extracelulare pe partea extracelulară și proteinele citoscheletice (de exemplu, microfilamentele de actină) în interiorul celulei. Acest lucru creează o conexiune între structurile intra- și extracelulare, ceea ce permite celulei să-și folosească propriul aparat contractil pentru a se mișca. În cele din urmă, există un grup mare de molecule care formează contacte celulare care realizează comunicarea între celule (joncțiuni interzise) și conexiuni mecanice (desmozomi, joncțiuni strânse).
Interacțiuni intercelulare la distanță realizat prin secretia de hormoni si factori de crestere (GF). Acestea din urmă sunt substanțe care au un efect stimulativ asupra proliferării și diferențierii celulelor și țesuturilor. Acestea includ, de exemplu, FR, obținut din trombocite și care afectează tranziția celulelor în faza de proliferare (miocite netede, fibroblaste, gliocite); FR epidermic - stimulează proliferarea celulelor epiteliale derivate din ectoderm; Fibroblast FR – stimulează proliferarea fibroblastelor. Se evidențiază în special un grup mare de peptide (somatotropine, somatomedine, insulină, lactogen) care afectează dezvoltarea celulelor fetale.
-
 Milano Metropolitan: harta, prețurile biletelor și sfaturi utile Cât costă biletele?
Milano Metropolitan: harta, prețurile biletelor și sfaturi utile Cât costă biletele?
-
 Învățați să citiți diagramele Jeppesen - Tutorial Instalarea suplimentelor care vor îmbunătăți semnificativ grafica și realismul simulatorului
Învățați să citiți diagramele Jeppesen - Tutorial Instalarea suplimentelor care vor îmbunătăți semnificativ grafica și realismul simulatorului
-
 Când și în ce cazuri ar trebui un antreprenor individual să depună o declarație zero?
Când și în ce cazuri ar trebui un antreprenor individual să depună o declarație zero?
-
 Ce este un epitet și cum să-l găsești?
Ce este un epitet și cum să-l găsești?










