Химиотерапия рака ободочной и прямой кишки. Химиотерапия. Мои страхи - что оправдалось, а что нет
В стандартную схему терапии, предназначенную для продления сроков жизни пациентов с онкологическими патологиями пищеварительных органов, в обязательном порядке входит химиотерапия. Этот широко используемый при устранении злокачественных новообразований метод заключается в проведении при помощи сильнодействующих лекарственных препаратов специфических лечебных мероприятий.
Обязательная химия при этом заболевании должна назначаться каждому конкретному пациенту строго индивидуально, в зависимости от общего состояния человека и наличия определённых клинических показателей, формы и стадии патологии, которые выявила . Правильно подобранные схема и курс противоопухолевой терапии помогают улучшить качество жизни онкобольного.
Традиционно многие годы применялось 2 вида химии:
монохимиотерапия. Данный метод заключается в проведении лечебного курса с помощью одного противоракового препарата и чаще всего применяется на 1 основного пищеварительного органа;
полихимиотерапия. Применение данной методики предусматривает назначение пациенту нескольких сильнодействующих лекарственных средств, которые тот должен принимать последовательно или одновременно.
Последний вид лечения, в котором используются достаточно сложные комбинации, составленные из нескольких противораковых лекарств, применяется чаще всего. Такое его преимущество заключается в возможности достижения в кратчайшие сроки максимального терапевтического эффекта, предусматривающего угнетение жизнедеятельности мутировавших клеток или их полную гибель.
Довольно часто в последние годы к химиотерапии стали относить таргетное, гормональное и иммунное лечение. Они являются высокоэффективными и менее травматичными для организма способами остановки мутации клеток. Виды такой терапии и их основные преимущества:
- Таргетная терапия. Останавливает размножение и рост и аномальных клеток благодаря целенаправленному воздействию на ДНК и рецепторы раковой опухоли.
- Иммунотерапия. Купирует развитие злокачественных клеток за счёт увеличившейся с помощью определённых лекарств способности иммунной системы выявлять и уничтожать чужеродных агентов.
- Гормонотерапия. Устраняет гормонозависимые опухоли, не поддающиеся уничтожению традиционной химией, посредством применения специальных гормональных препаратов.
Данные типы лечебных мероприятий с помощью сильнодействующих химиопрепаратов в современной клинической практике начинают выделять в самостоятельные разновидности противораковой терапии. Их стремительное развитие обусловлено как высокой результативностью, так и минимумом противопоказаний и побочных эффектов.
Особенности химии на разных этапах развития
В протоколы противоопухолевого комплекса при раковых новообразованиях в желудке, находящихся на 1-2 стадии развития, химия включается как вспомогательный курс, и может быть назначена как в предоперационный период, так и непосредственно во время хирургического вмешательства или после его. На этих этапах развития патологического состояния основного пищеварительного органа применяется комплексное терапевтическое воздействие несколькими противоопухолевыми фармацевтическими средствами, имеющими разный механизм воздействия. Эффективность, которую имеет химиотерапией, обуславливается тем, что активные лекарственные компоненты, вводимые с помощью капельного вливания и принимаемые перорально, распространяются по всему организму очень хорошо.
На последних этапах развития в основном пищеварительном органе раковой опухоли значение химии усиливается. Чаще всего онкобольным назначают системную терапию, хотя иногда рекомендуется и внутрибрюшинное введение цитостатических лекарств. Оно выполняется через маленький надрез, сделанный в брюшной стенке. Химиотерапия при раке желудка 4 стадии с метастазами предусматривает выделение таких видов лечебных мероприятий, как адьювантное, назначаемое после сделанной пациенту операции на основном пищеварительном органе или лучевого воздействия, и неоадъюватное, проводимое предварительно.
Химиотерапия при раке желудка на более поздней 3 стадии, имеет следующие разновидности:
- излечивающая или куративная, включающая адъювантную и неоадъювантную терапию. Применяется в том случае, когда допустимо оперативное вмешательство;
- паллиативная. Предназначается для прекращения роста неоперабельных опухолей.
На поздних стадиях ракового поражения часто назначается и самостоятельная противоопухолевая терапия. Необходимость её возникает только тогда, когда невозможна резекция новообразования или устранение его с помощью облучения. Эти виды химиотерапии при раке желудка применяются исключительно в стационаре, под непосредственным контролем врача. Они назначаются и в том случае, когда эффект от других методик отсутствует.
Адъювантная химиотерапия при раке желудка
Данная разновидность противоопухолевого лечения бывает, необходима после того, как на поражённом пищеварительном органе была проведена радикальная операция. Но стоит отметить, что такая химиотерапия после удаления желудка допустима только в том случае, когда у пациента отсутствуют клинические, гистологические и рентгенологические признаки остаточного патологического явления. Основной её целью является устранение метастаз микроскопического размера.
Адъювантная химиотерапия имеет предупреждающий характер, так как способна воздействовать на оставшиеся после операции отдельные аномальные клетки, циркулирующие по кровеносному руслу. Такой метод не является стандартом противоопухолевого лечения и применяется в основном как профилактическая химиотерапия после операции. Основной причиной для того, что данный вид терапевтических мероприятий используется не во всех случаях, является отсутствие специализированных средств для эффективного лечения желудочных опухолей.
После операций применяется и интраперитонеальная химиотерапия. Этот метод терапии используют только тогда, когда у онкобольного появляются признаки, свидетельствующие о распространении мутировавших клеток из основного пищеварительного органа на внутреннюю брюшную поверхность. Это приводит к развитию асцита (скопления в животе жидкости). Её специалисты во время проведения курса химии удаляют с помощью катетера. Через него же внутрь брюшины вливаются растворённые и подогретые до 40 °C препараты для химиотерапии. Дополнительно при интраперитонеальной химии для выведения лекарственных средств из организма онкобольным назначается в/в вливание жидкостей и противорвотные средства.
Неоадъювантная химиотерапия при раке желудка
Данный метод лечения в отличие от адъювантного проводится непосредственно до начала основного курса терапии. Его основной целью является уменьшение в размерах первичной опухоли для облегчения проведения операции и, следовательно, улучшения её результатов.
Стандартная неоадъювантная химиотерапия при раке желудка заключается в применении самой оптимальной схемы AC:
- Адриамицин, нередко используемым аналогом, которого является Доксорубицин. Лекарство назначается внутривенно, в дозе 45 мг/кв.м в сутки.
- Циклофосфамид. Химиотерапия перед операцией по удалению рака желудка этим препаратом проводится также с помощью в/в инъекций. Общепринятая его доза составляет 500 мг/кв.м в сутки.
Предоперационная химиотерапия по схеме AC предусматривает её шестикратное повторение с интервалом в 3 недели. Многих пациентов интересует вопрос о том, как рассчитываются площадь тела. Это обычно делают врачи во время назначения препарата, но для общей информации следует сказать, что для этого применяется формула Мостеллера. Смысл её заключается в том, что необходимо вывести корень квадратный из веса тела, в килограммах умноженного на рост в сантиметрах и разделённого на 3600.
Паллиативная химиотерапия
Питание при химиотерапии рака желудка должно быть ограниченным, так как онкобольные не могут воспринимать многие привычные продукты. В основном это относится к жирной и тяжёлой пище, горячим блюдам, а также соленьям и острым приправам. Недопустимо и употребление алкоголя, так как спиртные напитки легко могут спровоцировать возникновение рецидива.
Питание после химиотерапии предусматривает соблюдение определённых правил приёма пищи:
- основная масса продуктов на столе больного человека должна содержать повышенное количество минеральных и витаминных комплексов, а также белка;
- в питании необходимо соблюдать дробность, то есть кушать часто, но минимальными порциями;
- из ежедневного рациона следует исключить все блюда, в состав которых входят продукты с раздражающим действием.
Диета при химиотерапии рака желудка, назначенной в постоперационный период, должна непосредственно отвечать определённым требованиям. Основное значение в этом случае отводится потреблению важных для жизнедеятельности организма продуктов, содержащих минимум жиров и каких-либо химических микроэлементов, способных оказать раздражающее воздействие на слизистую пищеварительного органа.
Очень важным считается и контроль совместимости продуктов. Только в том случае, когда они будут идеально подходить друг к другу, снизится риск возникновения дополнительного повреждения желудка, способного спровоцировать рецидив болезни, сопровождающийся усилением болевых ощущений. Отдельно следует сказать о питании онкобольных с последней, запущенной стадией рака. Для того, чтобы поддерживать жизнедеятельность их организмов, им вводят внутривенно через капельницу, физраствор, протеины и глюкозу.
Как восстановить желудок после химиотерапии?
Несмотря на высокую эффективность химиотерапии, после её курса требуется специальное лечение, восстанавливающее работу повреждённых во время проведения терапевтических мероприятий органов. Основными задачами в этом случае становится нормализация функционирования внутренних систем организма, укрепление иммунитета человека и избавление его от интоксикации, то есть устранение нарушений, спровоцированных приёмом сильнодействующих препаратов.
Каждому конкретному пациенту необходима индивидуальная программа по восстановлению организма, которая включает в себя не только диету, но и лечебную физкультуру, плавание, лимфодренаж, арома- и сокотерапию, очистку организма травяными отварами.
Восстановление желудка после химиотерапии заключается в прохождение через определённые реабилитационные этапы:
- устранение общей выраженной интоксикации. Хорошие результаты достигаются при усилении питьевого режима отварами из ягод и целебных трав, а также регулярном приёме мочегонных фитосоставов;
- выведение из ЖКТ токсических веществ. Для этого применяются выделяющие слизь растения, например семя льна, алтей или дягиль, Полифепан и Активированный уголь;
- коррекция дисбактериоза. Для этого используют состав, приготовленный на основе комбинации таких трав, как цетрария исландская, чабрец ползучий и багульник болотный;
- восстановление в пищеварительных органах микрофлоры проводится живыми штаммами полезных бактерий, которые в больших количествах содержатся в определённых молочнокислых продуктах.
Восстановительная программа при устранении из пищеварительного органа злокачественных новообразований требуется даже в том случае, когда химиотерапия при раке желудка подобрана специалистом грамотно, и включает в себя только современные высокоэффективные препараты, позволяющие не допустить возникновения большинства возможных побочных эффектов.
Пациенты нередко интересуются тем, как проходит химиотерапия при раке желудка? Знание ответа на этот вопрос позволяет онкобольному человеку быть готовым ко всем нюансам этого метода лечения. По утверждению ведущих специалистов, применяемые для него лекарственные средства способны не только повлечь за собой большое количество негативных последствий, но привести к значительным ухудшениям в общем состоянии пациента.
Именно поэтому лечащие врачи перед назначением определённого курса тщательно взвешивают все «За» и «Против». Также в ходе проведения такого лечения онкологами в целях контроля эффективности проводятся регулярные диагностические обследования. Они дают возможность внести в терапевтический курс необходимые корректировки.
Информативное видео:
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
Химиотерапия рака желудка.
С.А. Тюляндин
Успехи химиотерапии рака желудка скромны. Очевидна необходи-мость поиска новых эффективных противо-опухолевых препаратов и их комбинаций.
В данной работе будет рассмотрена роль лекарственного метода лечения у боль-ных раком желудка и, в частности, значение химиотерапии при лечении диссеминированных больных и проведении предоперационной терапии у больных с местно-распространенным процессом, а также возможности адъювантной химиотерапии операбельного рака желудка.
Диссеминированный рак желудка
Нужно ли проводить химиотерапию у больных метастатическим раком желудка?
Возможно, кому-то этот вопрос покажется неуместным, однако в своей практике мы часто встречаем больных, которым было рекомендовано отказаться от проведе-ния химиотерапии. Особый скептицизм в отношении возможностей химиотерапии демонстрируют хирурги, работающие в общехирургических стационарах. В основе такого скептицизма лежит неспособность современной химиотерапии излечивать больных раком желудка. Однако рандомизированные исследования, в которых срав-нивались результаты химиотерапии и симптоматической терапии, убедительно про-демонстрировали тот факт, что лекарственная терапия увеличивает продолжитель-ность жизни у больных метастатическим процессом с 3-5 мес до 10-12 мес (табл. 1). На основании результатов этих исследований сегодня считается неэтичным отказы-вать больному диссеминированным раком желудка в проведении химиотерапии.
Таблица 1. Сравнение эффективности химиотерапии и симптоматической терапии у больных метастатическим раком желудка
|
Число больных |
Продолжительность жизни |
|
|
FAMTX |
10 мес |
|
|
Симптоматическая терапия |
3 мес |
|
|
FBMTX |
12 мес |
|
|
Симптоматическая терапия |
3 мес |
|
|
ELF |
10 мес |
|
|
Симптоматическая терапия |
4 мес |
|
|
ELF |
10,2 мес |
|
|
Симптоматическая терапия |
5 мес |
Эффективность различных противоопухолевых препаратов при раке желудка
В табл. 2 приведена частота объективных эффектов при назначении различных противоопухолевых препаратов у больных метастатическим раком желудка. Эффек-тивность их не превышает 30%, что свидетельствует о низкой чувствительности рака желудка к имеющимся в нашем распоряжении препаратам. До недавнего времени основным препаратом для лечения рака желудка был 5-фторурацил. Сейчас все боль-шую популярность завоевывают цисплатин, таксаны, иринотекан.
Что эффективнее: 5-фторурацил или комбинации?
До сих пор не существует убедительных доказательств того, что монотерапия 5-фторурацилом менее эффективна, чем комбинированная химиотерапия с вклю-чением или без включения 5-фторурацила. В литературе имеются лишь два рандо-мизированных исследования (табл. 3), в которых сравнивается эффективность 5-фто-рурацила и комбинаций на его основе. Было показано, что при проведении
Таблица 2. Эффективность различных противоопухолевых препаратов у больных диссеминированным раком желудка
|
Препараты |
Число больных |
Объективный эффект, % |
|
Антиметаболиты: |
||
|
5-фторурацил |
416 |
|
|
метотрексат |
||
|
гемцитабин |
||
|
UFT |
188 |
|
|
гидроксимочевина (per os) |
||
|
фторафур (per os) |
||
|
Антибиотики: |
||
|
митомицин-С |
211 |
|
|
доксорубицин |
141 |
|
|
эпирубицин |
||
|
Производные платины: |
||
|
цисплатин |
139 |
|
|
карбоплатин |
||
|
Таксаны: |
||
|
паклитаксел |
||
|
доцетаксел |
123 |
|
|
Ингибиторы топоизомеразы: |
||
|
иринотекан |
||
|
топотекан |
комбинированной химиотерапии чаще отмечается объективный противоопухолевый эффект, что, однако, не приводит к увеличению продолжительности жизни по сравнению с использованием монотерапии 5-фтор-урацилом. Следует признать, что небольшое число больных, участвовавших в этих исследованиях, не по-зволяет говорить о статистической достоверности по-лученных результатов. Вместе с тем, в большинстве стран мира возможность достижения большего проти-воопухолевого эффекта склонила чашу весов в пользу назначения комбинированной химиотерапии.
Какая схема комбинированной химиотерапии является стандартной для проведения химиотерапии первой линии?
Ответ на этот вопрос в разных странах и на разных кон-тинентах будет различен. Ни одна из изученных в рандо-мизированных исследованиях комбинация не продемон-стрировала убедительных преимуществ перед другими. Проще говоря, ни одна из них не является достаточно эф-фективной для лечения рака желудка. Многие из предло-женных комбинаций первоначально демонстрировали впечатляющие результаты. Однако при проведении рандо-мизированных исследований ни одна из них не смогла подтвердить полученных ранее результатов (табл. 4).
В 80-е годы наибольшей популярностью пользова-лась комбинация FAM (5-фторурацил, доксорубицин и митомицин-С), эффективность которой в первых ис-следованиях составила более 40% . Однако при про-ведении рандомизированных исследований продолжи-тельность жизни при использовании FAM и 5-фторурацила была одинаковой , а в более поздних исследованиях эффективность комбинации FAM умень-шилась до 9-25%. В начале 90-х годов после проведе-ния рандомизированного исследования, в котором ком-бинация FAM продемонстрировала худшие результаты, ей на смену пришла комбинация FAMTX (5-фторурацил, доксорубицин, метотрексат) . Комбинация FAMTX считалась стандартной для проведения химиотерапии диссеминированного рака желудка. При сравнении ее
Таблица 3. Результаты сравнения эффективности 5-фторурацила и комбинаций на его основе у
больных метастатическим раком желудка
|
Число больных |
Объективный эффект, % |
Продолжительность жизни, мес |
|
|
5-ФУ |
|||
|
5-ФУ+доксорубицин |
|||
|
FAM |
|||
|
5-ФУ |
7,5 |
||
|
FAM |
|||
|
103 |
Таблица 4. Результаты рандомизированных исследований у больных метастатическим раком желудка
|
Литературный источник |
Режим |
Число |
Объективный |
Продолжительность |
|
больных |
эффект, % |
жизни, мес |
||
|
Wils J. и соавт.(1991) |
FAM |
103 |
7,2 |
|
|
FAMTX |
105 |
10,5* |
||
|
Kelsen D. и соавт. (1991) |
FAMTX |
|||
|
EAP |
||||
|
Vanhoefer U. и соавт. (2000) |
FAMTX |
6,7 |
||
|
ELF |
7,2 |
|||
|
7,2 |
||||
|
Cocconi G. и соавт. (2001) |
FAMTX |
200 |
6,9 |
|
|
PELF |
7,7 |
|||
|
Webb A. и соавт. (1997) |
FAMTX |
130 |
6,1 |
|
|
ECF |
126 |
8,7 * |
* p<0.05.
с комбинацией EAP (этопозид, доксорубицин, циспла-тин) при равной эффективности FAMTX оказалась ме-нее токсичной .
В конце 90-х годов все чаще стали использоваться комбинации с включением платины. Одним из таких режимов является комбинация PF, в которой после вве-дения цисплатина предусмотрена пролонгированная инфузия 5-фторурацила в течение 5 сут.
В исследовании EORTC решено сравнить эффектив-ность комбинаций FAMTX, PF и ELF (этопозид, лейко-ворин, 5-фторурацил) . ELF был предложен для ле-чения пожилых и ослабленных больных как обладающий минимальной токсичностью, и пользует-ся популярностью в связи с простотой проведения и возможностью амбулаторного лечения. Результаты были разочаровывающими. Эффективность всех трех комбинаций не превышала 20%, а средняя продолжи-тельность жизни была одинаковой и составила около 7 мес. Авторы сделали вывод, что ни одна из изученных комбинаций не может считаться стандартной для про-ведения химиотерапии у больных диссеминированным раком желудка и подчеркивали необходимость разра-ботки новых комбинаций.
Другая цисплатин-содержащая комбинация PELF (цисплатин, эпирубицин, лейковорин и 5-фторурацил) также не смогла доказать свое преимущество перед ре-жимом FAMTX, при этом частота побочных эффектов в группе PELF была выше .
Сегодня известны результаты только одного иссле-дования, в котором комбинация FAMTX продемонстри-ровала более скромные результаты по сравнению с цис-платин-содержащей комбинацией ECF (эпирубицин, цисплатин, длительные инфузии 5-фторурацила) . Частота объективных эффектов (46% и 21%) и средняя продолжительность жизни (8,7 и 6,1 мес) были досто-верно лучше для ECF. Таким образом, комбинации с включением цисплатина лишь незначительно улучши-ли прогноз больных метастатическим раком желудка.
Приведенные выше данные позволяют говорить об отсутствии стандартов лекарственного лечения боль-ных метастатическим раком желудка. PF считается стан-дартной в США, Корее и Японии, в то время как в Евро-пе чаще используется ECF. Многие, считая комбинации с включением цисплатина слишком токсичными, пред-почитают использовать «бесплатиновые» режимы (ELF или FAMTX). По непосредственной эффективности пла-тиновые комбинации имеют некоторые преимущества, которые, однако, не влияют существенным образом на продолжительность жизни больных диссеминированным раком желудка.
Выбор того или иного режима должен определяться конкретной клинической ситуацией и, в частности, об-щим состоянием больного. Так, при лечении пациентов молодого возраста в общем удовлетворительном состоя-нии без сопутствующих осложнений, таких как кровоте-чение, мы предпочитаем назначать режимы с включени-ем платины, например MEP . У лиц пожилого возраста и ослабленных больных предпочтительной является ком-бинация ELF, которая обладает умеренной токсичностью и может осуществляться в амбулаторных условиях.
Как улучшить результаты химиотерапии?
В последние годы возрос интерес к применению так-санов и иринотекана для лечения больных раком желуд-ка. В монотерапии эффективность этих препаратов со-ставила 21-23%. Комбинация доцетаксела и цисплатина оказалась эффективной у 16 (37%) из 39 больных при средней продолжительности жизни 10,4 месяца .
В исследовании E. Van Cutsem и соавт. была постав-лена задача определить оптимальную комбинацию с включением доцетаксела у больных раком желудка. При сравнении комбинации ТС (доцетаксел и цисплатин) и TCF (доцетаксел, цисплатин и 5-фторурацил) обе комби-нации продемонстрировали высокую противоопухоле-вую эффективность (частота объективных эффектов со-ставила 35% и 56% соответственно) и значительную продолжительность времени до прогрессирования (5,0 и 5,9 месяца соответственно) при равной частоте побочных эффектов. На основании этого комбинация TCF была выб-рана для тестирования в сравнительном рандомизирован-ном исследовании, в котором больные контрольной груп-пы будут получать цисплатин и инфузии 5-фторурацила.
В другом кооперированном исследовании проведено сравнение эффективности и токсичности комбинации IP (иринотекан и цисплатин) и IFU (иринотекан, лейково-рин и 5-фторурацил) у больных распространенным ра-ком желудка . Частота объективных эффектов в груп-пе IP составила 28%, в группе IFU - 39%, что послужило основанием для дальнейшего изучения комбинации IFU в рамках рандомизированного исследования. Таким об-разом, возможно, результаты проводимых в настоящее время рандомизированных исследований определят зна-чение доцетаксела и иринотекана в комбинированной химиотерапии диссеминированного рака желудка.
Изучается также возможность применения в составе комбинированной химиотерапии новых пероральных представителей фторпиримидинов (капецитабина, UFT), которые по своим фармакокинетическим пара-метрам имитируют длительные внутривенные инфузии 5-фторурацила. В связи с этим логичной представляет-ся замена в комбинации ECF столь утомительных для персонала и пациентов пролонгированных инфузий 5-фторурацила на пероральный прием капецитабина или UFT. Показано, что капецитабин в дозе 1000 мг/м 2 дважды в день в комбинации с цисплатином в дозе 60 мг/м 2 в 1-й день и эпирубицином в дозе 50 мг/м 2 каж-дые 3 нед обладает удовлетворительной переносимос-тью и эффективен у 39% больных с аденокарциномой желудка . Анализ фармакокинетики показал, что ка-пецитабин хорошо усваивается даже у больных, пере-несших ранее резекцию желудка, при этом концентра-ция препарата в крови аналогична таковой при проведении длительных внутривенных инфузий 5-фто-рурацила.
Для лечения 50 больных метастатическим раком же-лудка была использована комбинация с включением эпирубицина 50 мг/м 2 в 1-й день, цисплатина 60 мг/м 2 в 1-й день и UFT 360 мг/м 2 перорально ежедневно в те-чение 21 дня с одновременным приемом лейковорина внутрь в дозе 45 мг, повторный курс лечения проводи-ли на 28-й день . Частота объективных эффектов изу-ченной комбинации составила 54,3% при средней про-должительности жизни 10 мес. Преимуществом предложенной комбинации является удобный прием фторпиримидинов per os вместо инфузий 5-фторура-цила в классическом режиме ECF.
Можно ли продлить достигнутый на фоне проводи-мой химиотерапии противоопухолевый эффект у боль-ных раком желудка с помощью ингибиторов ангиоге-неза? J. Fielding и соавт. продемонстрировали результаты рандомизированного исследования, в кото-ром изучалась эффективность нового антиангиогенно-го препарата из группы ингибиторов металлопротеи-наз - маримастата . В исследовании приняли участие 369 больных диссеминированным раком же-лудка с объективными эффектами или стабилизацией болезни на момент окончания химиотерапии. В момент прекращения химиотерапии им назначали плацебо или маримастат. Прием маримастата достоверно увеличил время до прогрессирования со 135 дней в группе пла-цебо до 167 дней в группе маримастата. Одногодичная выживаемость составила 14% и 20% соответственно.
Вторая линия химиотерапии при раке желудка
Сегодня не существует общепринятых рекомендаций по проведению второй линии химиотерапии у больных диссеминированным раком желудка. Могу лишь поде-литься опытом нашего отделения. Если в качестве хи-миотерапии первой линии была использована комби-нация с включением цисплатина (например MEP, PF или TPF), то при прогрессировании процесса чаще всего назначается комбинация ELF. Если же на первом этапе была использована комбинация ELF, то в качестве хи-миотерапии второй линии при общем удовлетвори-тельном состоянии назначаются комбинации с вклю-чением цисплатина (цисплатин-митомицин-С). Кроме того, для проведения второй линии химиотерапии мо-гут быть использованы пероральные фторпиримидины, например, капецитабин, UFT или фторафур.
Местнораспространенный рак желудка
При раке желудка T3-4 выполнение радикальной опе-рации является технически сложной задачей. Кроме того, на этой стадии первичной опухоли высока вероятность метастазирования в регионарные лимфатические узлы. В связи с этим становится оправданным проведение нео-адъювантной химиотерапии, которая, в случае успеха улучшает возможности выполнения радикальной опера-ции и уничтожает отдаленные микрометастазы. К сожа-лению, целесообразность такого подхода пока не под-тверждена данными соответствующих исследований. В двух рандомизированных исследованиях неоадъювант-ная химиотерапия не привела к существенному увеличе-нию частоты выполнения радикальных резекций и со-ответственно к улучшению отдаленных результатов по сравнению с оперативным лечением без предшествую-щей лекарственной терапии . В данных исследова-ниях в качестве химиотерапии использовали комбина-ции FAMTX и PF, которые, как уже было показано ранее, обладают незначительным противоопухолевым эффек-том при раке желудка. Именно низкой эффективностью использованных комбинаций можно объяснить неуда-чи неоадъювантной терапии. Хочется надеяться, что вне-дрение в практику новых комбинаций с включением так-санов, иринотекана и других препаратов повысит результативность неоадъювантной терапии у больных местнораспространенным раком желудка. Очень важно также определить факторы, которые будут предсказывать эффективность планируемой химиотерапии у конкрет-ного больного.
Операбельный рак желудка
Прогноз больных операбельным раком желудка оп-ределяется, в первую очередь, стадией заболевания. Бо-лее 80% больных с T1-2N0M0 выздоравливают после ра-дикальных операций. Показатель 5-летней выживаемости падает до 50% при наличии T3 и состав-ляет не более 20% при наличии метастазов в регионар-ные лимфатические узлы. С этих позиций не вызывает сомнений необходимость проведения адъювантной системной терапии у больных операбельным раком желудка .
Однако на сегодняшний день не существует убеди-тельных данных о пользе проведения адъювантной те-рапии у больных операбельным раком желудка. В лите-ратуре существуют отдельные сообщения об улучшении
Таблица 5. Результаты рандомизированных исследований адъювантной терапии у больных операбельным раком желудка .
|
Литературный источник |
Режим |
Число |
Продолжительность |
5-летняя |
|
больных |
жизни, мес |
выживаемость, % |
||
|
Allum W. и соавт (1989) |
Митомицин-С-5ФУ |
141 |
||
|
Митомицин-С-5ФУ-CMFP |
140 |
|||
|
Контроль |
130 |
|||
|
Coombes R. и соавт. (1990) |
FAM |
133 |
||
|
Контроль |
130 |
|||
|
Nakajima T. и соавт. (1999) |
Митомицин-С-UFT-araC |
288 |
||
|
Контроль |
285 |
|||
|
Hallissey M. и соавт. (1994) |
Контроль |
145 |
||
|
ЛТ (СОД 46 Гр) |
138 |
|||
|
FAM |
159 |
|||
|
Ducreux M. и соавт. (2000) |
5-ФУ |
127 |
||
|
Контроль |
133 |
|||
|
Di Bartolomeo M. и соавт. (2000) |
EAP-5-ФУ |
137 |
||
|
Контроль |
137 |
безрецидивной и общей выживаемости при использо-вании митомицина-С, однако ни одно большое рандо-мизированное исследование не подтвердило целесооб-разность адъювантной терапии у этой категории больных.
I. Panzini и соавт. представили результаты мета-ана-лиза 17 рандомизированных исследований, посвящен-ных изучению роли адъювантной химиотерапии, в ко-торые в общей сложности были включены 2913 больных с резектабельным раком желудка . Исполь-зование химиотерапии в сочетании с хирургическим лечением уменьшило риск смерти на 14% по сравнению с оперативным лечением без химиотерапии. Эти ре-зультаты указывают на весьма скромное улучшение вы-живаемости в группе больных, получивших адъювант-ную химиотерапию.
В табл. 5 приведены результаты рандомизированных исследований по адъювантной терапии рака желудка с участием более 100 больных в каждой из сравниваемых групп. Ни одно из них не показало улучшения отдален-ных результатов лечения при проведении адъювантной терапии с использованием комбинаций, включающих митомицин-С или производные платины. В исследова-нии M. Hallissey и соавт. в качестве адъювантной тера-пии проводили лучевую терапию (СОД-46 Гр), что ухуд-шило результаты лечения по сравнению с контролем.
Единственным исследованием, показавшим целесо-образность адъювантной терапии после радикальной резекции желудка, является исследование SWOG-Intergroup . 603 больных аденокарциномой желуд-ка или пищеводно-желудочного соединения Ib-IV ста-дий после радикальной операции были рандомизированы на две группы. В первой группе па-циенты не получали адъювантного лечения. Во второй группе получали лечение по следующей схеме:
- 1 курс химиотерапии 5-фторурацилом 425 мг/м 2 и лейковоринам 20 мг/м 2 1-5-й день
- 1 укороченный курс химиотерапии 5-фторураци-лом 400 мг/м 2 и лейковорином 20 мг/м 2 1-4-й день в 1-ю неделю лучевой терапии
- лучевая терапия суммарная доза 45 Гр фракциями по 1,8 Гр
- 1 укороченный курс химиотерапии 5-фторураци-лом 400 мг/м 2 и лейковорином 20 мг/м 2 1-3-й день в последнюю неделю лучевой терапии
Таблица 6. Результаты адъювантной химиолучевой терапии в сравнении с наблюдением у больных раком желудка после оперативного лечения
|
Наблюдение |
ХТ+ЛТ |
|
|
Число больных |
275 |
281 |
|
Длительность безрецидивного периода |
19 мес |
30 мес |
|
Продолжительность жизни |
28 мес |
35 мес |
|
3-летняя выживаемость |
40% |
50% |
|
4-летняя выживаемость |
30% |
46% |
|
Первые рецидивы: |
||
|
в оставшейся части желудка или анастомозе |
29% |
19% |
|
регионарные лимфатические узлы |
72% |
68% |
|
отдаленные метастазы |
18% |
35% |
- 2 курса химиотерапии 5-фторурацилом 425 мг/м 2 и лейковорином 20 мг/м 2 1-5-й день спустя 1 мес.
Хотя химиолучевое лечение было токсичным, в целом оно признано переносимым. Зарегистрировано 3 случая смерти от токсичности; токсичность III-IV степени от-мечена у 73% больных (гематологическая, гастроинтес-тинальная, инфекционная). Результаты исследования после 4 лет наблюдения представлены в табл. 6.
Таким образом, это исследование показало достовер-ное улучшение на 10% 3-летней выживаемости у боль-ных, получавших адъювантную комбинированную те-рапию, за счет уменьшения числа рецидивов заболевания в оставшейся части желудка и прогресси-рования за счет отдаленных метастазов. Возможно, та-кая схема лечения станет новым стандартом терапии больных раком желудка с высоким риском рецидива (II и III стадии) после радикально выполненного оператив-ного лечения.
Внутрибрюшинное введение противоопухолевых препаратов
С этой целью используются цисплатин в дозе 75-100 мг, блеомицин 60 мг, ТиоТЭФ 40-60 мг. При таком спо-собе введения в брюшной полости создается высокая концентрация противоопухолевых препаратов на дли-тельный срок. Не имеет смысла внутрибрюшинное вве-дение циклофосфана, поскольку циклофосфан сам по себе не обладает противоопухолевой активностью. Только в печени под действием фермента Р-450 цикло-фосфан превращается в метаболит фосфарамид мус-тард, обладающий противоопухолевой активностью.
По аналогии с циклофосфаном лишено смысла и внутрибрюшинное введение 5-фторурацила, который только в печени превращается в обладающий противо-опухолевой активностью 5-фтор-2‘-дезоксиуридинмо-нофосфат (FdUMP).
Сегодня нет сведений относительно того, что внут-рибрюшинное введение противоопухолевых препара-тов адъювантно после радикально выполненных опе-раций улучшает результаты лечения. Показанием к внутрибрюшинному введению цитостатиков является накопление асцита, обусловленного опухолевой диссе-минацией по брюшине, с целью прекращения или уменьшения скорости его накопления. Перед введени-ем препаратов следует произвести максимально воз-можное удаление асцита и ввести противоопухолевые препараты, разведенные в 100-200 мл изотонического раствора NaCl.
Опасности проведения химиотерапии у больных раком желудка
Химиотерапия рака желудка чревата серьезными ос-ложнениями, обусловленными как токсичностью самих противоопухолевых препаратов, так и особенностями течения заболевания. В частности, при раке желудка отмечается потеря массы тела, которая должна прини-маться во внимание при планировании химиотерапии. Быстрая потеря массы тела в течение последнего меся-ца или общая потеря ее более 10% от исходного являет-ся крайне неблагоприятным фактором. У таких боль-ных проведение химиотерапии осложняется развитием глубокой, нередко фебрильной нейтропенией, сепси-са, стоматита, энтероколита, сопровождающегося тяже-лой диарей. При выборе химиотерапии у таких боль-ных предпочтение следует отдать бесплатиновым ком-бинациями, уменьшив дозы препаратов на 25-50% уже при проведении первого курса.
Крайним проявлением нарушения питания является выраженная или полная дисфагия вследствие стеноза или отказ от приема пищи в связи с «отвращением» к ней. Не следует проводить химиотерапию «голодному» больному. Надо, прежде всего, разрешить стеноз и до-биться стабилизации массы тела больного, а затем пла-нировать химиотерапию. Больным с потерей массы тела на фоне химиотерапии следует проводить парен-теральное питание. Для стимуляции аппетита и в нашем отделении назначается мегейс в дозе 240-320 мг ежед-невно перорально. Прибавка массы тела на фоне про-ведения химиотерапии является важным показателем ее эффективности, в то время как потеря массы тела часто является первым симптомом неудачи проводимого ле-чения.
Другая опасность при проведении химиотерапии -кровотечение из неудаленной первичной опухоли же-лудка или рецидива в зоне анастомоза. Это осложнение является угрозой для жизни больного и нередко сопро-вождает успешное проведение химиотерапии вслед-ствие распада опухоли. При проведении химиотерапии у больных с неудаленным первичным очагом или реци-дивом в желудке следует тщательно контролировать уровень гемоглобина не реже 2-3 раз в неделю. Боль-ной должен быть предупрежден о возможности разви-тия у него мелены или рвоты сгустками крови и необ-ходимости немедленного оповещения в этом случае медицинского персонала. При появлении признаков кровотечения химиотерапия должна быть прекращена, а все усилия следует сосредоточить на симптоматичес-кой гемостатической терапии, вплоть до кровезамести-тельной. После остановки кровотечения продолжать химиотерапию следует только на фоне гемостатичес-кой терапии.
Нередко кровотечение из распадающейся опухоли желудка является показанием к выполнению паллиатив-ной гастрэктомии или резекции желудка. Если речь идет
0 больном молодого возраста в общем удовлетворитель-ном состоянии, кровотечение из распадающейся опу-холи желудка является показанием для выполнения опе-ративного лечения до начала проведения химиотерапии.
Заключение
Успехи химиотерапии рака желудка скромны. Оче-видна необходимость поиска новых эффективных про-тивоопухолевых препаратов и их комбинаций. Опре-деление молекулярных особенностей клеток опухоли рака желудка определит новые мишени для целевого воздействия препаратов, блокирующих рецепторы фак-торов роста и пути передачи пролиферативных сигна-лов, воздействующих на механизмы контроля клеточ-ного цикла и поддержания целостности генома, ингибирующих опухолевый ангиогенез. Появление эф-фективных режимов для лечения метастатических форм рака желудка сделает оправданным их примене-ние на более ранних стадиях заболевания в качестве неоадъювантной и адъювантной терапии.
Литература
1. Ван де Велде К. Хирургическое и лекарственное лечение операбельного рака желудка: результаты двух рандомизированных исследований Голландской группы по раку желудка. Материалы II ежегодной Российской онкологической конференции, М., 8-10 декабря 1998 г. - М, 1999. - С. 43-44.
2. Allum W.H., Hallissey M.T., Kelly K.A. Adjuvant chemotherapy in operable gastric cancer: 5-year follow-up offirst British Stomach Cancer Group trial// Lancet. - 1989. -Vol. 1.- P. 571-574.
3. Bazin I.S., Garin A.M., Zharkov S.A. Response to cisplatin based combinations in patients with advanced gastric cancer. Second International Conference on Biology, Prevention and Treatment of Gastrointestinal Malignancies. - Koln, 1995. -PP.56.
4. Cocconi G, Carlini P., Gamboni A. et al. PELF is more active than FAMTXin metastatic gastric carcinoma (MGC)//Proc. ASCO-2001.
Vol. 20. - (Abstract 501).
5. Coombes R.C., Schein P.S., Chilvers C.E. et al. A randomized trial comparing adjuvantfluorouracil, doxorubicin, and mitomycin with no treatment in operable gastric cancer. International Collaborative Cancer Group// J. Clin. Oncol. - 1990. - Vol. 8. - P. 1362-1370.
6. Cullinan S, Moertel C, Fleming T. et al. A comparison of three chemotherapeutic regimens in the treatment of advanced pancreatic and gastric carcinoma// JAMA.. - 1985. - Vol. 253. - P. 2061-2067.
7. Di Bartolomeo M., Bajetta E, Bordogna G. et al. Improved adjuvant therapy outcome in resected gastric cancer patients according to node involvement: 5-year results of a randomized study by the Italian Trials in Medical Oncology (ITMO)// Proc. ASCO. -2000. - Vol. 19. - Abstr.
934.
8. Ducreux M., Nordiner B., Ychou M. et al. Resected Gastric Adenocarcinoma: randomized trial of adjuvant chemotherapy with 5FU-cisplatyin//Ibid. - Abstr. 932.
9. Evans T., Paul J., McInnes A. et al. A phase I and PK study of capecitabine in combination with epirubicin and cisplatin in patients with advanced oesophagogastric adenocarcinoma// Ibid. -2001. -Vol. 20. - Abstr. 651.
10. Fielding J., Scholefield .J, Stuart R. A randomized double-blind placebo-controlled study of marimastat in patients with inoperable gastric adenocarcinoma// Ibid-2000. - Vol. 19. - Abstr. 929.
11. Hallissey M.T., Dunn J.A., Ward L.C., Allum W.H. The second British Stomach Cancer Group trial of adjuvant radiotherapy or chemotherapy in resectable gastric cancer: five-year follow-up// - Lancet. - 1994. - Vol. 343 - P. 1309.
12. Kang Y.K., Choi D.W., Im Y.H. et al. A phase III randomized comparison of neoadjuvant chemotherapy followed by surgery versus surgery for locally advanced stomach cancer// Proc ASCO. - 1996. - Vol. 15. - P. 215.
13. Karpeh M.S., Kelsen D.P., Tepper J.E. Cancer of the Stomach// Cancer: Principles and Practice of Oncology. - New-York: Lippincott Williams & Wilkins, 2001. - P. 1092-1126.
14. Kelsen D., Atiq O., Saltz L. et al. FAMTX (fluorouracil, methotrexate, Adriamycin) is as effective and less toxic than EAP (etoposide, Adriamycin, cisplatin): a random assignment trial in gastric cancer// Proc ASCO. - 1991. - Vol. 10. - P. 137.
15. Kim N.K., Park Y.S., Heo D.S., et al. A phase III randomized study of 5-fluorouracil alone in the treatment of advanced gastric cancer// Cancer (Philad.). - 1993. - Vol. 71(12). - P. 3813.
16. Kim S., Yeul H., Shin F. et al. Phase II trial of epirubicin (E), cisplatin (P), oral UFT and leucovorin (L) in advanced gastric carcinoma (AGC) patients. Program and abstracts of the 25th Congress of the European Society for Medical Oncology; October 13-17, 2000; Hamburg, Germany. - Abstr. 274.
17. Macdonald J., Schein P., Woolley P. et al. 5-Fluorouracil, doxorubicin, and mitomycin (FAM) combination chemotherapy for advanced gastric cancer// Ann. Intern. Med. - 1980. - Vol. 93. - P. 533-536.
18. Macdonald J.D., Small S., Benedetti J. et al. Postoperative combined radiation and chemotherapy and improves disease-free survival (DFS) and overall survival (OS) in resected adenocarcinoma of the stomach and GE junction: results ofMergm^ Study INT-0116 (SWOG9008)/
/ Proc. ASCO. - 2000. - Vol. 19. - Abstr. 1.
19. Nakajima T., Nashimoto A., Kitamura M. et al. Adjuvant mitomycin and fluorouracil followed by oral uracil plus tegafur in serosa-negative gastric cancer: a randomised trial. Gastric Cancer Surgical Study Group// Lancet. - 1999. - Vol. 354. - P. 273.
20. Panzini I., Gianni L. et al. Adjuvant chemotherapy and gastric cancer: meta-analysis of 17 randomized trials. Program and abstracts of the 25th Congress of the European Society for Medical Oncology; October 13-17, 2000; Hamburg, Germany. - Abstr. 273.
21. Pozzo C., Bugat R., Peschel C. et al. Irinotecan in combination with CDDP or 5-FU and folinic acid is active in patients with advanced gastric or gastro-oesophageal junction adenocarcinoma: final results of a randomised phase IIstudy// Proc. ASCO. - 2001, - Vol. 20. - Abstr.
531.
22. Ridwelski K., Gebauer T., Fahlke J. et al. Combination chemotherapy with docetaxel and cisplatin for locally advanced and metastatic gastric cancer// Ann. Oncol. - 2001. - Vol. 12. - P. 47-51.
23. Van Cutsem E.J.D., Ajani J., Tjulandin S. et al. Docetaxel in combination with cisplatinum with or without 5-fluorouracil in patients with advanced gastric or GE junction adenocarcinoma: preliminary results. Program and abstracts of the 25th Congress of the European Society for Medical Oncology; October 13-17, 2000; Hamburg, Germany. - Abstr. 276.
24. Vanhoefer U., Rougier P., Wilke H. et al. Final results of a randomized phase III trial of sequential high-dose methotrexate, fluorouracil, and doxorubicin versus etoposide, leucovorin, and fluorouracil versus infusional fluorouracil and cisplatin in advanced gastric cancer: A trial of the European Organization for Research and Treatment of Cancer Gastrointestinal Tract Cancer Cooperative Group// J. Clin. Oncol. - 2000.
Vol. 18. - P. 2648-2657.
25. Webb A., Cunningham D., Scarffe J.F. et al. Randomized trial comparing epirubicin, cisplatin, and fluorouracil versus fluorouracil, doxorubicin, and methotrexate in advanced esophagogastric cancer// Ibid. - 1997. - Vol. 15. - 261-267.
26. Wils J., Klein H., Wagener D. et al. Sequential high-dose methotrexate and fluorouracil combined with doxorubicin: A step ahead in the treatment of advanced gastric cancer-A trial of the EORTC Gastrointestinal Tract Cooperative Group// Ibid. - 1991. - Vol. 9. - P. 827-831.
27. Wils J. The treatment of advanced gastric cancer// Semin. Oncol. - 1996. - Vol. 23. - P. 397-403.
Practical oncology
C.A. Тюляндин
Приложение 1.
Комбинации, используемые для лечения рака желудка
FAM
- 5-фторурацил 600 мг/м 2 1, 8, 29, 36-й дни
- Доксорубицин 30 мг/м 2 внутривенно 1, 29-й дни
- Митомицин-С 10 мг/м 2 1-й день Повторение курса каждые 8 нед. FAMTX
- Метотрексат 1500 мг/м 2 инфузия 30 мин 1-й день
- 5-фторурацил 1500 мг/м 2 инфузия 30 мин через 1 ч после метотрексата
- Лейковорин 30 мг внутривенно или внутрь через 24 ч после введения метотрексата каждые 6 ч 8 доз
- Доксорубицин 30 мг/м 2 внутривенно 15-й день Повторный курс лечения на 22-й день.
EAP
- Этопозид 120 мг/м 2 внутривенно 4, 5, 6-й дни
- Доксорубицин 20 мг/м 2 внутривенно 1-й и 7-й дни
- Цисплатин 40 мг/м 2 внутривенно 2-й и 8-й дни Повторный курс лечения на 29-й день.
- Цисплатин 100 мг/м 2 внутривенно 1-й день
- Фторурацил в суточной дозе 1000 мг/м 2 внутривенная инфузия 1-5-е сутки Лечение проводится каждые 28 дней.
ELF
- Этопозид 120 мг/м 2 внутривенно 1, 2, 3-й дни
- Лейковорин 30 мг/м 2 внутривенно 1, 2, 3-й дни
- 5-фторурацил 500 мг/м 2 внутривенно струйно 1, 2, 3-й дни Курс лечения повторяют на 28-й день.
PELF
- цисплатин 40 мг/м 2 внутривенно 1-й и 5-й дни;
- эпирубицин 30 мг/м 2 внутривенно 1-й и 5-й дни
- лейковорин 100 мг/м 2 внутривенно 1-4-й дни
- 5-фторурацил 300 мг/м 2 внутривенно 1-4-й дни Курс лечения каждые 4 нед.
ECF
- эпирубицин 50 мг/м 2 внутривенно каждые 3 нед
- цисплатин 60 мг/м 2 внутривенно каждые 3 нед
- 5-фторурацил в суточной дозе 200 мг/м 2 постоянная внутривенно инфузия в течение 18-21-й нед ТС
- цисплатин 75 мг/м 2 внутривенно 1-й день Повторение курса каждые 3 нед
- доцетаксел 75 мг/м 2 внутривенно 1-й день
- цисплатин 75 мг/м 2 внутривенно 1-й день
- 5-фторурацил в суточной дозе 750 мг/м 2 внутривенно инфузия 1-5-е сутки Курс лечения проводится каждые 3 нед.
- иринотекан 200 мг/м 2 внутривенно 1-й день
- цисплатин 60 мг/м 2 внутривенно 1-й день Курс лечения проводится каждые 3 нед
IFU
- иринотекан 80 мг/м 2
- лейковорин 500 мг/м 2 2 ч
- 5-фторурацил 2000 мг/м 2 инфузия в течение 22 ч Еженедельно 6 нед с повтором после недельного интервала. МЕР
- Митомицин 5 мг/м 2 внутривенно 1-й и 7-й дни
- Этопозид 60 мг/м 2 внутривенно 4, 5, 6-й дни
- Цисплатин 40 мг/м 2 внутривенно 2-й и 8-й дни Курс лечения каждые 4 нед.
Химиотерапия – метод лечения онкологии, применяющий цитостатические (противоопухолевые) препараты.
Чаще используется системный подход, лекарства поступают в кровоток и циркулируют по всем органам организма, разрушая патологические клетки. Но также задействуется и регионарная химиотерапия, когда лечение получают конкретные участки тела.
Больница Асаф-ха-Рофэ предоставляет услуги химиотерапевтического лечения в рамках терапии онкологических заболеваний. Это самое крупное государственное медицинское учреждение в Израиле. Здесь иностранный пациент сможет получить медицинскую помощь, соответствующую самым высоким мировым стандартам.
Записаться на консультацию
Химиотерапия при раке прямой кишки в Израиле
Лечение цитостатическими средствами рака прямой кишки в отделении онкологии Асаф проводят:
До хирургии с/без облучения, чтобы сократить величину опухоли. Особую пользу она приносит, когда злокачественное образование находится вблизи анального сфинктера. Если воздействие цитостатиков позволит уменьшить опухоль прямой кишки, врач может сохранить сфинктер.
После оперативного вмешательства, с/без радиотерапии, чтобы разрушить оставшиеся патологические сегменты и сократить риск возврата болезни. Ослабить проявления метастатического опухолевого процесса. Здесь химиотерапия при раке прямой кишки применяется как основной метод лечения, когда вторичные очаги возникают в печени или легких, чтобы контролировать болезнь, сколько будет возможно.
Главные применяемые цитостатические препараты:
- фторурацил (5-ФУ) – дают как внутривенную инъекцию, с перерывами или как непрерывную инфузию;
- кселоду® (Xeloda®) (в виде таблеток);
- иринотекан* (Irinotecan*) (внутривенно);
- ралтитрексед (внутривенно).
Схемы химиопрепаратов при раке прямой кишки:
- 5-ФУ и лейковорин (calcium folinate).
- Лейковорин повышает результативность 5-ФУ.
- FOLFOX – элоксатин в комплексе с 5-ФУ и лейковорином.
- Эта схема примененяется также вместе с бевацизумабом.
- FOLFIRI - иринотекан в комплексе с 5-ФУ и фолиевой кислотой.
- FOLFIRI также даётся вместе с авастином.
- FOLFOXIRI - иринотекан, оксалиплатин, 5-ФУ и фолиевая кислота.
- Иринотекан и капецитабин также назначают вместе с авастином.
- Оксалиплатин и капецитабин могут объединить с авастином.
Если препараты первой линии терапии не оказывают должного эффекта, врачи применяют другие цитостатические средства:
- Цетуксимаб (Эрбитукс) – препарат таргетной терапии дают вместе с иринотеканом и назначают, когда первичное или вторичное лечение не оказало необходимого эффекта.
- Цетуксимаб использование обусловлено тем, какие лекарства были применены в качестве первичного лечения, и дал ли генетический тест положительный результат на мутации гена KRAS.
- Если мутации находят, цетуксимаб не назначают, так как его действие направлено на рецепторы эпидермального фактора роста EGFRs. Они способствуют развитию патологических клеток.
- Панитумумаб (Vectibix) – препарат таргетной терапии, предназначенный для терапии метастатического рака прямой кишки, который ранее лечили с помощью 5-ФУ, иринотекана или оxaliplatinа.
Получить консультацию врача
 Такой вид терапии цитостатиками называется адъювантным. Задача лечения – помочь предотвратить рецидив рака или его распространение на другие части тела. В течение операции хирург увидит, насколько глубоко рак врос в стенку кишечника или окружающие ткани, выяснить, объем опухоль. Образцы отправляются в лабораторию для дальнейшего изучения.
Такой вид терапии цитостатиками называется адъювантным. Задача лечения – помочь предотвратить рецидив рака или его распространение на другие части тела. В течение операции хирург увидит, насколько глубоко рак врос в стенку кишечника или окружающие ткани, выяснить, объем опухоль. Образцы отправляются в лабораторию для дальнейшего изучения.
Факторы, свидетельствующие о вероятности возврата болезни:
- Злокачественные клетки находят в удаленных лимфоузлах во время операции.
- Рак распространился на кровеносные сосуды (васкулярная инвазия).
- Опухолевый процесс проник глубоко в стенку кишечника или поразил окружающие ткани.
В таких ситуациях злокачественные клетки отрываются от первичной опухоли в прямой кишке и разносятся по кровотоку или лимфатической системе. Они слишком маленькие, чтобы клетки распознавались с помощью томографии, но при этом способны образовать вторичные опухоли.
Химиопрепараты эффективны, если злокачественные образования малого размера, нежели крупного. Поэтому врач рекомендует лечение цитостатиками после операции, чтобы снизить вероятность его возврата или распространения. Лекарство по кровотоку проходит по всему телу, уничтожая злокачественные клетки.
Химиотерапию начинают через 8 недель примерно, когда пациент придет в себя после операции.
Препараты химиотерапии при раке прямой кишки после хирургии:
- FOLFOX - сочетание фолиевой кислоты (лейковорина), фторурацила и оксалиплатина (внутривенное введение).
- Капецитабин (кселода) – в таблетках.
- Фторурацил (5-ФУ) – внутривенно.
- XELOX - сочетание оксалиплатина и капецитабина
Может потребоваться лечение от 6 до 7 месяцев. Химиопрепараты могут быть в виде таблеток, которые возможно принимать дома. Либо это внутривенная терапия с помощью канюли, центрального катетера, системы PICC line или portacath (кат-порт).
Химиотерапия при распространенном раке прямой кишки
Терапия цитостатиками не избавит пациента от распространенного рака прямой кишки, но способна уменьшить опухолевый процесс и увеличить выживаемость. Задачи лечения – замедлить развитие болезни и управлять ее симптомами – болью, потерей аппетита и веса.
На поздних стадиях рака главная цель терапии – помочь пациенту чувствовать себя лучше. Поэтому если побочные эффекты имеют выраженный характер, лечение прекращают.
Химиопрепараты, которые применяют для лечения рецидива или распространенного рака прямой кишки:
- Капецитабин (кселода) (таблетки)
- Фторурацил (5-ФУ)
- Ралтитрексед в вену.
- Ралтитрексед рекомендуют при противопоказаниях к 5-ФУ или капецитабину.
- Оксалиплатин
- Иринотекан
Врачи применют несколько различных комбинаций этих препаратов, в том числе:
- FOLFOX
- FOLFIRI
- XELOX (оксалиплатин и капецитабин).
При выборе препаратов врач принимает во внимание различные факторы, чтобы найти оптимальный вариант. Он учитывает, какое лечение проводилось ранее, и сколько времени потребовалось, чтобы болезнь вернулась. Онколог обсуждает варианты терапии с пациентом.
Если рак возвращается, применяют другие цитостатики, лечение носит название терапия второй линии.
Постоянно проводятся испытания, чтобы улучшить лечение прогрессирующего рака прямой кишки.
Узнать стоимость лечения
Как проверяется эффективность курса химиотерапии при раке прямой кишки?
Перед началом лечения врач проводит сканирование, затем спустя 3 месяца. Измеряется величина опухоли, поэтому через время определяется, насколько хорошо работает лечение. Варианты:
- Злокачественно образование уменьшилось.
- Осталось такого же размера.
- Увеличилось.
Если объем опухоли остался прежним, доктор поговорит с пациентом по вопросу продолжения лечения – стоит или не стоит его продолжать.
Когда она уменьшилась или осталась прежней, потребуется терапия еще в 4-6 месяцев. Лечение продолжается, пока не возникает слишком большого количества побочных эффектов. Терапию останавливают на время. Врач расскажет о преимуществах и недостатках различных вариантов. Обычно каждые 2-3 месяца проводят КТ, чтобы определить эффективность лечения.
Если опухоль стала крупнее, химиотерапию остановят и порекомендуют другой метод.
Химиотерапия и операция по удалению метастазов в печени.
 Иногда врачи рекомендуют проведение хирургического вмешательства, чтобы удалить вторичные очаги в печени.
Иногда врачи рекомендуют проведение хирургического вмешательства, чтобы удалить вторичные очаги в печени.
Оперативное вмешательство выполняют, если нет никаких других признаков рака в организме. Для этого проводят ПЭТ-КТ, чтобы отыскать злокачественные клетки за пределами печени.
Когда опухоль в печени слишком большая, чтобы её удалить, рекомендуют курс химиотерапии при раке прямой кишки с целью уменьшить величину новообразования. Лечение цитостатиками проводится как до, так и после операции.
Если стандартная химиотерапия при метастазах неэффективна, предлагается лечение в рамках клинических испытаний.
Лечение химиопрепаратами применяется в данном случае:
- Чтобы разрушить раковые клетки, которые проникли в печень, но не развились в опухоль.
- С целью уничтожить злокачественные сегменты, которые, возможно, остались после операции по удалению опухоли в печени.
- Чтобы сократить величину злокачественного образования в печени перед хирургией, сделать возможным удалением неоперабельной опухоли.
Флоксуридин (Floxuridine, FUDR) – препарат, похожий на 5-ФУ, вводят через крошечные катетеры, установленные в печеночную артерию. Лекарство также подают более длительное время с помощью помпы, вживленной в область печени. Этот вид регионарной химиотерапии при раке прямой кишки называется печеночной артериальной инфузией.
Регионарную терапию флоксуридином также могут чередовать с внутривенной химиотерапией 5-ФУ. Преимущество регионарной химиотерапии состоит в том, что она обеспечивает высокую концентрацию цитостатика к опухоли и обычно приводит к меньшим нежелательным последствиям лечения в остальных частях организма. Минус заключается в отсутствии воздействия на злокачественные клетки, которые могут находиться за границами данного органа.
Заказать обратный звонок
Химиолучевая терапия рака прямой кишки
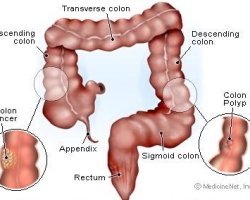 Это заболевание часто лечат, применяя облучение до или после операции. Такая методика помогает предотвратить рецидив. Радиотерапия уменьшает опухоль, облегчая процесс удаления.
Это заболевание часто лечат, применяя облучение до или после операции. Такая методика помогает предотвратить рецидив. Радиотерапия уменьшает опухоль, облегчая процесс удаления.
Также применятся химиотерапия при раке прямой кишки одновременно с лучевой терапией. Цитостатики делают злокачественные клетки боле чувствительными к радиации.
Так как лечение является комбинированным, вероятнее всего, что оно будет более успешным, чем радиотерапия сама по себе. В таких случаях используют химиопрепараты – фторурацил (5-ФУ), капецитабин.
5-ФУ поступает в организм:
- С помощью капельницы.
- Посредством помпы, которую пациент носит 24 часа в сутки.
- В виде серии инъекций в вену перед лучевой терапией.
Капецитабин пациент принимает в форме таблеток утром и вечером во время облучения.
Сочетание радиотерапии и химиотерапии усугубляет побочные эффекты. Комбинированное лечение повысит утомляемость. Также у пациента иногда возникает диарея, тошнота, слабая устойчивость к инфекции, частое мочеиспускание, раздражение кожи в области обработки.
Потенциальные побочные эффекты после химиотерапии при раке прямой кишки
Уничтожая раковые клетки, химиопрепараты убивают здоровые, подверженные быстрому делению и росту. Клетки крови, поэтому лечение цитостатиками снизит количество лейкоцитов, эритроцитов и тромбоцитов. Это означает следующее:
- Пациент чувствует себя уставшим.
- Повысится вероятность инфекции.
- Человек становится подверженным различным видам кровотечений.
Если развивается температура выше 38°C или признаки инфекции, важно немедленно обратиться в больницу. Иногда потребуется срочное лечение антибиотиками.
Повышенная усталость – наиболее распространенный побочный эффект у людей, проходящих химиотерапию. Пациент может испытывать слабость, недостаток энергии. Такое состояние отмечается в течение нескольких месяцев после окончания лечения. На сколько быстро человек вернется к нормальной жизни, зависит от общего состояния здоровья, проведенной ранее терапии и процедур, которые планируются.
Другие возможные отрицательные последствия химиотерапии включают:
- тошноту;
- диарею;
- стоматит;
- потерю или истончение волос;
- изменения в менструальном цикле;
- боль в глазах, ощущение, как будто в них насыпали песок.
Чаще при данном заболевании применяют следующие химиопрепараты:
- фторурацил;
- фолиевую кислоту;
- ралтитрексед;
- иринотекан;
- оксалиплатин.
Получить программу лечения
Побочные эффекты фторацила (5-ФУ)
Большинство людей хорошо справляется с приемом данного препарата, наблюдается мало побочных эффектов, наиболее распространенные из них:
- тошнота;
- усталость;
- диарея;
- снижение эритроцитов;
- стоматит.
Если 5-ФУ поступает в организм с помощью помпы, иногда появляется покраснение и болезненность кистей и стоп - ладонно-подошвенная эритема. Возникает у 1 из 3 пациентов. Кожа шелушится на ладонях рук и подошвах ног. У основной массы больных данный симптом достаточно мягкие, и лечение продолжается. Если состояние ухудшается, врач снижает дозу препарата или порекомендует сделать перерыв, пока больной не выздоровеет.
Побочные эффекты капецитабина (кселоды)
Последствия капецитабина очень похожи на побочные эффекты 5-ФУ, также возникает покраснение и болезненность рук и ног - ладонно-подошвенную эритему.
Чаще симптом – мягко выраженный, если пациенту становится хуже, дозировку кселоды снижают или предлагают сделать перерыв, пока больной не восстановиться.
Побочные эффекты ралтитрекседа (томудекса)
Этот цитостатик назначают для лечения больным, когда нет возможности принимать фторурацил или капецитабин. Это может быть связано с проблемами сердца, например, стенокардией.
Общие побочные эффекты томудекса включают:
- Снижение кровяных клеток.
- Диарею, которая возникнуть через несколько дней после начала лечения.
- Побочный эффект бывает достаточно серьезным, поэтому важно, сразу уведомить врача.
- Усталость.
- Тошноту.
- Стоматит, включая боль в горле и затрудненное дыхание.
- Изменения в работе печени, как правило мягкие, чтобы вызывать симптомы.
- Врач проводит регулярный анализ крови для проверки функционирования органа.
- Кожную сыпь.
- Расстройства желудка и боль.
Побочные эффекты иринотекана
К общим нежелательным последствиям терапии препаратом относят:
- Повышенное потоотделение.
- Усталость.
- Слезящиеся глаза.
- Тошноту.
- Истончение или выпадение волос.
- Снижение клеток крови.
- Увеличение воспроизводства слюны.
- Схваткообразные боли в животе.
- Диарею.
У некоторых людей наблюдается потливость, боли в животе и диарея во время терапии. Чтобы уменьшить побочные эффекты, врач назначает препарат атропин, делают подкожную инъекцию.
Диарея после иринотекана бывает серьезным побочным эффектом. О возникновении этого симптома необходимо обязательно уведомить врача. Иногда потребуется прием противодиарейных лекарств. Врач может назначить антибиотик, если диарея усиливается. Иногда, очень быстро наступает обезвоженность, поэтому следует связаться с врачом сразу.
Побочные эффекты оксалиплатина
К общим нежелательным последствиям лечения относят:
- тошноту;
- онемение губ;
- чувствительность к холоду;
- онемение и покалывание в руках и стопах.
Онемение и покалывание возникает, поскольку оксалиплаин влияет на нервы. Ощущение холода длиться несколько дней после приема препарата. Иногда, симптом становится более серьезной проблемой, если лечение препаратом длилось достаточно долго. Некоторые люди отмечают, что им трудно ходить, потому что подошвы ног немеют.
Необходимо сообщить врачу, если возникло покалывание или онемение, особенно, когда эти проявления не уходят. Следует снизить дозу препарата или остановить терапию на время. Можно использоваться другие химиопрепараты. У некоторых людей этот побочный эффект становится постоянным.
Записаться на лечение
|
Фаза курса химиотерапии |
||
|
интенсивная |
продолжения |
|
|
4**** H R* / 4 H 3 R 3 * 6 H R** / 6 H 3 R 3 ** 6 H Z E*** / 6 H 3 Z 3 E 3 *** |
||
|
2 H R Z E S + 1 H R Z E |
5 H R E / 5 H 3 R 3 E 3 6 H R E*** / 6 H 3 R 3 E 3 *** |
|
|
3 H R Z E /[K] |
В соответствии с режимами I, IIа или IV в зависимости от лекарственной чувствительности микобактерий |
|
|
4 H R/ 4 H 3 R 3 |
||
|
Минимум 5 препаратов, к которым сохранена чувствительность Длительность фазы не менее 6 мес |
Минимум 3 препарата, к которым сохранена чувствительность Длительность фазы не менее 12 мес |
|
Примечания.
* При туберкулезе органов дыхания
** При внелегочном туберкулезе, при туберкулезе любых локализаций у детей и подростков
*** При туберкулезе любых локализаций у детей и подростков
**** Продолжительность курса химиотерапии в месяцах
Сокращения: H – изониазид, R – рифампицин, Z – пиразинамид, E – этамбутол, S – стрептомицин, Rb – рифабутин, K – канамицин/амикацин, Pt – протионамид, Cap – капреомицин, Fq – препараты из группы фторхинолонов, Cs – циклосерин, PAS – ПАСК
Возможные варианты режимов и включения в них отдельных препаратов указаны после знака " / ". В квадратных скобках приведены режимы и препараты, назначение которых основывается на данных о лекарственной чувствительности микобактерий.
3.1. Первый (I ) режим химиотерапии назначают впервые выявленным больным с бактериовыделением и/или распространенным либо осложненным поражением различных органов.
В фазе интенсивной терапии назначают 4 основных препарата: изониазид, рифампицин, пиразинамид и стрептомицин или этамбутол. Последний лучше назначать в регионах с частой устойчивостью микобактерий туберкулеза к стрептомицину 1 . Интенсивную фазу химиотерапии продолжают не менее 2 месяцев. За этот срок больной должен принять 60 доз комбинации из 4 основных препаратов. В случае пропуска приема полных доз длительность фазы интенсивной терапии увеличивают до приема 60 доз.
Через 2 месяца от начала лечения вопрос о переходе ко второму этапу решает Клинико-экспертная комиссия (КЭК) на основании данных клинико-рентгенологического и микробиологического исследования.
При сохраняющемся после 2 месяцев химиотерапии бактериовыделении (по микроскопии мокроты) фазу интенсивной терапии можно продолжить еще на 1 месяц (30 доз) до получения данных о лекарственной чувствительности возбудителя. В зависимости от результата проводят коррекцию химиотерапии и продолжают (по решению КЭК) фазу интенсивной терапии. При невозможности исследования лекарственной чувствительности и/или при отрицательной клинико-рентгенологической динамике процесса после 3 месяцев химиотерапии больного направляют в вышестоящее учреждение для исследования лекарственной чувствительности и определения дальнейшей тактики ведения. В ожидании результатов лечение проводят в соответствии с интенсивной фазой терапии.
При тяжелом и осложненном течении туберкулеза любой локализации продолжительность фазы интенсивной терапии может быть увеличена по решению КЭК.
При отрицательных результатах микроскопии мокроты после 2 месяцев химиотерапии и положительной клинико-рентгенологической динамике переходят к фазе продолжения химиотерапии.
В фазе продолжения терапии назначают 2 основных препарата - изониазид и рифампицин – в течение 4 месяцев (при туберкулезе органов дыхания) или в течение 6 месяцев (при внелегочном туберкулезе) ежедневно или в интермиттирующем 2 режиме (3 раза в неделю). Другим режимом в фазе продолжения может быть ежедневный прием изониазида и этамбутола в течение 6 мес. При туберкулезном менингите у взрослых фаза продолжения лечения длится 8-12 месяцев.
Детям и подросткам в фазе продолжения лечения назначают в течение 6 мес. изониазид и рифампицин или изониазид, пиразинамид и этамбутол ежедневно или в интермиттирующем режиме (3 раза в неделю). Фаза продолжения может быть увеличена до 9 месяцев у детей и подростков с генерализованным туберкулезом, туберкулезным менингитом, при сохраняющейся более 6 месяцев деструкции легочной ткани без бактериовыделения, а также у детей в возрасте до 3 лет включительно. Эти больные в фазе продолжения могут получать 3 препарата: изониазид, рифампицин и пиразинамид или этамбутол.
3.2. Второй А (II a ) режим химиотерапии назначают при повторном курсе химиотерапии после перерыва в лечении или по поводу рецидива при невысоком риске лекарственной устойчивости микобактерий туберкулеза.
В фазе интенсивной терапии назначают 5 основных препаратов: изониазид, рифампицин, пиразинамид, этамбутол и стрептомицин. Через 2 месяца (60 принятых суточных доз) терапию продолжают 4 препаратами (изониазид, рифампицин, пиразинамид, этамбутол) в течение еще 1 месяца (30 доз). Общая длительность интенсивной фазы – не менее 3 месяцев (90 суточных доз комбинации лекарств). В случае пропуска приема полных доз длительность интенсивной фазы увеличивают до приема 90 доз.
Через 3 месяца. от начала фазы интенсивной терапии вопрос о переходе ко второму этапу лечения решает КЭК на основании данных клинико-рентгенологического и микробиологического исследования.
При сохранении бактериовыделения и невозможности исследования лекарственной чувствительности микобактерий туберкулеза и/или при отрицательной клинико-рентгенологической динамике процесса через 3 месяца больного направляют в вышестоящее учреждение для исследования лекарственной чувствительности и определения дальнейшей тактики ведения. До получения результатов лечение проводят как в интенсивной фазе терапии.
При отрицательных результатах микроскопии мокроты через 3 месяца химиотерапии и положительной клинико-рентгенологической динамике приступают к фазе продолжения химиотерапии. К этому сроку, как правило, получают данные о лекарственной чувствительности микобактерий туберкулеза, которые могут потребовать коррекции химиотерапии.
При чувствительности микобактерий туберкулеза к основным химиопрепаратам в фазу продолжения терапии еще в течение 5 месяцев назначают изониазид, рифампицин и этамбутол ежедневно или в интермиттирующем 1 режиме (3 раза в неделю). Общая продолжительность терапии – 8 месяцев. Для детей и подростков фаза продолжения лечения составляет 6 месяцев, общая продолжительность терапии – 9 месяцев.
3.3. Второй Б (II б) режим химиотерапии назначают больным с высоким риском лекарственной устойчивости микобактерий до получения результатов микробиологического исследования. К их числу относятся:
больные, у которых отсутствует эффект от химиотерапии либо имеет место обострение или прогрессирование процесса на фоне лечения;
больные, не получавшие ранее противотуберкулезные препараты, но у которых имеются веские основания для предположений о лекарственной устойчивости по анамнестическим и/или клиническим данным (контакт с больными, выделяющими микобактерии туберкулеза с множественной лекарственной устойчивостью, остро прогрессирующее течение).
В фазе интенсивной терапии в течение 3 месяцев назначают комбинацию из 4 основных препаратов (изониазид, рифампицин/рифабутин, пиразинамид, этамбутол) и 2-3 резервных (в зависимости от данных о лекарственной устойчивости по региону).
Дальнейшее лечение корректируют на основании данных о лекарственной чувствительности микобактерий туберкулеза и проводят в соответствии с режимами Первым (I), Вторым А (II a) или Четвертым (IV).
Данный режим лечения может быть использован в противотуберкулезных учреждениях, имеющих лабораторную службу с действующим механизмом контроля качества и возможностью определения лекарственной устойчивости к препаратам резерва.
3.4. Третий (III ) режим химиотерапии назначают впервые выявленным больным без бактериовыделения, с малыми (ограниченными) и неосложненными формами туберкулеза.
В фазе интенсивной терапии назначают 4 основных препарата: изониазид, рифампицин, пиразинамид, этамбутол. Детям назначают 3 основных препарата: изониазид, рифампицин и пиразинамид или стрептомицин, или этамбутол (последний не назначают детям дошкольного возраста). Интенсивную фазу продолжают 2 месяца. За этот срок больной должен принять 60 доз комбинации из 4 (у детей – из 3) основных препаратов. В случае пропуска приема полных доз длительность фазы интенсивной терапии увеличивают до приема 60 доз.
Через 2 месяца от начала интенсивной фазы терапии вопрос о переходе ко второму этапу лечения решает КЭК на основании данных клинико-рентгенологического и микробиологического исследования.
При появлении бактериовыделения (по микроскопии мокроты) и/или в случае отрицательной клинико-рентгенологической динамики процесса после 2 месяцев лечения необходимы определение лекарственной чувствительности микобактерий туберкулеза и соответствующая коррекция химиотерапии. В ожидании результатов лечение не меняют в течение 1 месяца. При невозможности исследования лекарственной чувствительности больного направляют в вышестоящее учреждение. Режим дальнейшего лечения определяют с учетом лекарственной чувствительности возбудителя. У детей при замедленной положительной клинико-рентгенологической динамике процесса интенсивную фазу лечения можно продлить на 1 месяц.
При положительной клинико-рентгенологической динамике и отсутствии микобактерий туберкулеза по данным микроскопии мокроты переходят к второму этапу лечения – фазе продолжения.
В фазе продолжения терапии назначают 2 основных препарата - изониазид и рифампицин – в течение 4 месяцев ежедневно или в интермиттирующем 1 режиме (3 раза в неделю). Другим режимом в фазе продолжения может быть прием изониазида и этамбутола в течение 6 месяцев.
Ремиссии при этом могут продолжаться 8-9 месяцев. Лечение первичных или рецидивных опухолей желудка, которые не могли быть удалены хирургически, более эффективно, чем метастазов рака желудка К препарату чувствительны метастазы рака желудка в печень, яичники, лимфоузлы брюшной полости! меньше - лимфоузлы малого таза.
Можно достичь удовлетворительных результатов при раке толстой и особенно прямой кишки, однако ремиссии здесь менее длительны.
Фторурацил можно назначать после операции с целью профилактики рецидивов и метастазов.
Способ применения. Фторурацил применяют внутривенно, в виде 20% -ной мази, а также в виде внутриартериальных или внутривенных инфузий и регионарной перфузии.
Согласно американским инструкциям, фторурацил чаще всего применяется внутривенно из расчета 10-15 мг на 1 кг массы тела. Препарат вводится в этой дозе один раз в день в течение 4-5 дней подряд, если не отмечено токсических проявлений, в последующие дни 4-5 раз вводят половинную дозу препарата - 7,5 мг на 1 кг массы тела через день.
При проявлении первых признаков интоксикации (стоматит, диарея) лечение прекращают. После окончания курса, независимо от наличия или отсутствия токсических явлений, продолжать лечение этим же препаратом не рекомендуется. Ежедневная доза фторурацила не должна превышать 1 г.
Состояние после химиотерапии
В связи с тем что после применения такой методики лечения фторурацилом часто возникают тяжелые токсические осложнения, в Институте экспериментальной и клинической онкологии АМН СССР разработана более щадящая методика. Последняя предусматривает введение фторурацила через день, что позволяет применить более высокую суммарную дозу препарата и значительно уменьшить побочное его действие.
Препарат вводится внутривенно (быстро), из расчета 15 мг на 1 кг массы тела в день. Дневная доза - 0,75-1,5 г. Инъекции производятся через день. Суммарная доза на курс лечения составляет 3-5 г, а при отсутствии побочных явлений - до 7,5 г.
Если препарат переносится больным хорошо, через 4-6 недель рекомендуется повторить курс лечения с целью продлить ремиссию. Общее количество применяемого препарата зависит от реакции больного на предыдущий курс лечения. Некоторые больные могут получать до 5, а иногда и более курсов. При такой схеме лечения токсические проявления выражены нерезко и легко могут быть устранены.
Количество курсов определяется эффективностью проводимого лечения и выраженностью побочных явлений. При наличии объективного, субъективного или симптоматического эффекта (уменьшение размеров опухоли, определяемое пальпацией или рентгенологически, улучшение общего состояния, исчезновение болей и других симптомов болезни), курсы химиотерапии фтору рацилом повторяют до тех пор, пока удается поддерживать этот эффект. В случае отсутствия эффекта и прогрессирования процесса дальнейшее назначение препарата нецелесообразно.
Периодичность сеансов химиотерапии
После лечения фторурацилом у больных отмечается уменьшение размеров опухоли, вплоть до полной регрессии. Ремиссия длится обычно 5-8 недель, несколько месяцев, а иногда год и более. После окончания химиотерапии воспользуйтесь препаратом Фотостим , его свойства предотвращают появление новых опухолей.
Лучших результатов можно добиться при сочетании лечения фторурацила с лучевой терапией, особенно при раке легких, пищевода и поджелудочной железы.














