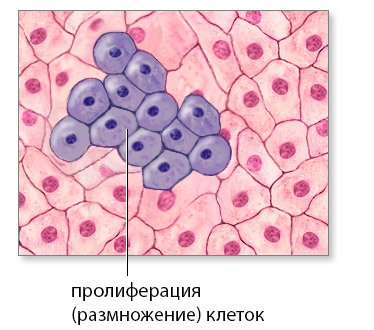
Научная электронная библиотека. Эмбриональный гистогенез. Пролиферация клеток. Клеточный рост, миграция и межклеточные взаимодействия
ПРОЛИФЕРАЦИЯ (от лат. proles-потомство и f его--несу), термин., введенный Вирховым для обозначения новообразования клеток путем. их размножения делением. Как понятие общее и весьма широкое П. может относиться к процессам самого различного характера. Так, П. клеток лежит в основе регенеративного новообразования тканей (см. Регенерация); П. наблюдается при различных гиперплазиях (см. Гиперплазия); наконец П. клеток лежит в основе опухолевого разрастания ткани. Естественно, что такие пролиферативные процессы могут иметь место в самых разнообразных тканях, однако способность тканевых элементов к П. далеко не одинакова: чем более высоко диференцированы клетки, тем в меньшей степени они способны к П.;в частности в комплексных тканях, напр. в эпителии, П. исходит почти как правило из тех тканевых зон, к-рые состоят из менее диференцированных элемен- тов; такие зоны принято называть пролифера-ционными центрами или центрами роста. В многослойном плоском эпителии пролифера-ционному центру соответствует зона Мальпи-гиевого или зародышевого слоя, в железах- места переходов выводных протоков в железистые пузырьки. Следствием П. обычно бывает образование новой ткани (продукция ткани),. впрочем это не является правилом: например элементы, происходящие в результате воспалительной П., часто не строят новую ткаяь, а лишь пронизывают, инфильтрируют окружающую ткань.
Под пролиферацией понимают процесс деления клеток, приводящий к увеличению объема ткани. Наиболее активно пролиферация происходит в эмбриональном периоде, когда клетки формирующегося зародыша непрерывно и интенсивно делятся. Этот процесс регулируется гормонами и биологически активными субстанциями, которые способны как усиливать ее (факторы роста), так и ослаблять.
Увидеть термин «пролиферация» в заключениях специалистов, многие тот час же пытаются найти значение этого слова, одновременно испытывая беспокойство по поводу возможного неблагополучия, однако паниковать не стоит: пролиферация – это еще не болезнь .
Клетки многих тканей нуждаются в постоянном обновлении, это естественный физиологический процесс, реализуемый посредством деления. Особенно выражено обновление клеток в коже, слизистых оболочках пищеварительного тракта, дыхательной системы, матки. То есть пролиферация в этих тканях – явление нормальное и необходимое.
С другой стороны, чрезмерное размножение клеток не может считаться нормой и приобретает патологические черты.
Наиболее часто пролиферация служит проявлением воспалительного процесса (гастрит, цервицит), повреждений (после операций, травм), опухоли. Усиление пролиферации лежит в основе разрастания тканей в новообразованиях, при гиперпластических процессах. Предраковые изменения, в том числе дисплазия, также сопровождаются повышенной пролиферацией клеток.
 Если при воспалительных изменениях или травматических повреждениях пролиферация носит обычно преходящий характер и призвана восстановить ткань до нормы, то в случае опухолей она приобретает иное значение.
При новообразованиях пролиферация не только избыточна, но и безостановочна, клетки делятся непрерывно, приводя к появлению и росту опухоли. Предела такой пролиферации не существует, как нет предела и клеточному делению в опухоли.
Если при воспалительных изменениях или травматических повреждениях пролиферация носит обычно преходящий характер и призвана восстановить ткань до нормы, то в случае опухолей она приобретает иное значение.
При новообразованиях пролиферация не только избыточна, но и безостановочна, клетки делятся непрерывно, приводя к появлению и росту опухоли. Предела такой пролиферации не существует, как нет предела и клеточному делению в опухоли.
Пролиферация нередко сопровождается атипией, то есть размножающиеся клетки обретают несвойственные им черты, изменяются внешне и функционально. Атипия говорит о возможной предраковой трансформации. Появление у клеток нехарактерных черт при усиленной пролиферации неудивительно: быстрое размножение создает условия для генетических мутаций, а клетки не успевают как следует созреть. В этом случае количество не означает качество, и в стремительно размножающемся клоне клеток рано или поздно появляются аномальные, мутировавшие элементы.
Факт высокой вероятности атипии при клеточной пролиферации делает этот процесс потенциально опасным, поэтому врачи относятся к нему настороженно. Если клетки изменили свой вид или свойства, можно говорить о и нужно срочно принимать меры по ликвидации патологического очага.
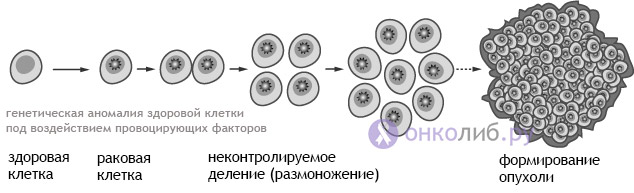
развитие рака — неконтролируемая пролиферация с атипией
В заключениях морфологов можно встретить указание на степень выраженности процессов пролиферации. Этот показатель довольно субъективен, ведь четких критериев, позволяющих отличить эти степени, не существует. Более того, в одних органах умеренная пролиферация может считаться нормой, в то время как в других даже слабое усиление клеточного деления вызывает беспокойство. В этой связи, пациентам не стоит слишком акцентироваться на степени, но если речь идет о патологической пролиферации, то понятно, что чем она сильнее, тем хуже.
Видео: о делении клеток и развитии рака
Пролиферация в гинекологии (эндометрия и шейки матки)
Пожалуй, наиболее часто с явлением пролиферации сталкиваются врачи акушеры-гинекологи. Деление клеток в женских половых органах очень активно происходит в норме и еще более интенсивно – при патологии. О наличии пролиферации говорится в заключении гистологического исследования слизистой оболочки тела матки или шеечного канала, фрагмента шейки, удаленного путем конизации.

На основании заключения гинеколог делает выводы о норме или патологии, а женщина, получающая результат на руки, стремится подробнее узнать о сути пролиферации. Не секрет, что многие специалисты не слишком разговорчивы и не пускаются в подробные объяснения смысла отдельных терминов, поэтому попробуем разобраться, что может означать пролиферация в матке и что с этим делать.
Матка в разных отделах имеет неодинаковое строение и различную выстилку. Так, шейка в наружной части покрыта многослойным плоским эпителием, цервикальный канал выстлан цилиндрическим, а слизистая тела органа (эндометрий) – сложно устроенная железистая ткань. На протяжении менструального цикла матка испытывает на себе колебания половых гормонов и готовится к потенциальной беременности, поэтому пролиферация – не только нормальный, но и жизненно необходимый механизм, обеспечивающий изменение эндометрия для комфортной имплантации.
Пролиферация многослойного плоского эпителия наружного отдела шейки матки имеет смысл только для обновления покровного слоя, поэтому в норме не должна быть слишком выражена. У беременных женщин вследствие гормональных перестроек обнаруживается умеренная пролиферация железистого эпителия шейки матки, что не считается патологией.
Усиление пролиферации эпителия может говорить о:
- Воспалительном процессе (цервицит);
- Травматическом повреждении (диагностическое выскабливание, аборты, удаление патологически измененных фрагментов шейки, разрывы при родах);
- Опухолевом росте ( , папилломы, дисплазия, ).
Таким образом, исходя из причинного фактора, условно в шейке матки выделяют пролиферацию воспалительную (цервицит), гиперпластическую (полипы, псевдоэрозии, опухоли) и посттравматическую (разрывы, рубцовые изменения).
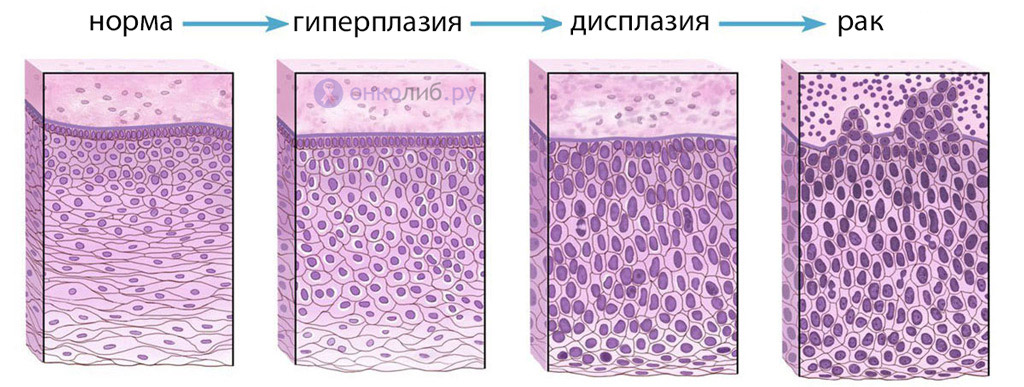
трансформация здоровой ткани в опухолевую
Различного рода цервициты (бактериальные, вирусные, грибковые) неминуемо ведут к повреждению покровного эпителия, который, стремясь восстановить свою целостность, начинает активно пролиферировать. На фоне этого выражены и другие признаки воспаления – инфильтрация клетками воспалительного ряда (лейкоциты, лимфоциты, макрофаги), расширение сосудов микроциркуляторного русла, отек, поэтому причина повышенного размножения клеток обычно ясна.
Сходные изменения происходят при истинной эрозии, повреждениях шейки матки в родах, при абортах, внутриматочных манипуляциях. Пролиферация отражает регенерацию (восстановление) многослойного плоского эпителия и скорее физиологична.
Ускоренное деление клеток при указанных выше изменениях обычно не опасно, хотя и требует лечения с последующим контролем его эффективности. Если слизистая восстановилась, то поводов для беспокойства нет.
Совсем другое значение приобретает пролиферация эпителия с атипией . В многослойном плоском покровном эпителии атипия часто сопутствует поражению онкогенными типами папилломавируса, когда риск злокачественной трансформации очень высок, а также псевдоэрозии шейки матки, в народе именуемой просто эрозией.
Псевдоэрозия – это появление в наружной части шейки матки железистого эпителия, подобного тому, который в норме выстилает шеечный канал. Процесс носит дисгормональный характер, часто протекает на фоне вирусного поражения и цервицита. Пролиферация в псевдоэрозиях касается как плоского эпителия, который врастает в эти очаги, стремясь их «нейтрализовать», так и цилиндрического, составляющего собственно эрозионные железы.
Избыточная пролиферация железистого эпителия в структурах псевдоэрозий приводит к образованию сосочков, разветвлений и новых желез в толще шейки. Размножение клеток плоского эпителия, стремящегося заместить аномальные железистые комплексы, нередко сопровождается дисплазией, а значит, процесс стал на путь формирования рака.
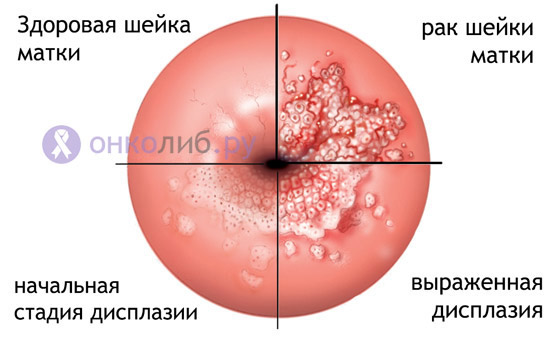 Пролиферация с дисплазией в многослойном плоском эпителии – наиболее опасное сочетание.
Усиленное размножение клеток, нарушение их правильной ориентации в толще эпителиального пласта, появление ненормальных внешних черт – все это признаки дисплазии, основного предракового процесса шейки матки.
Пролиферация с дисплазией в многослойном плоском эпителии – наиболее опасное сочетание.
Усиленное размножение клеток, нарушение их правильной ориентации в толще эпителиального пласта, появление ненормальных внешних черт – все это признаки дисплазии, основного предракового процесса шейки матки.
Цервикальный канал, ведущий внутрь матки, выстлан цилиндрическим эпителием, который тоже вполне способен к размножению. В норме пролиферация цилиндрического эпителия нужна для обновления клеток, но встречается и при патологии – воспаление, полипы шеечного канала, аденомы, карциномы.
Эндометрий – это внутренний слой тела матки, который имеет сложную организацию и непрерывно меняет свое строение на протяжении всего менструального цикла. В фазу десквамации (кровотечение) он отторгается, если беременность не наступила, а затем должен вновь образоваться и увеличиться в объеме. Так происходит постоянно. Понятно, что без пролиферации тут не обойтись, клетки должны активно делиться, восстанавливая слущенный при менструации эндометрий.
Пролиферация клеток эндометрия наиболее активно происходит в первую половину цикла, которую так и называют – фаза пролиферации. В этот период слизистая матки находится под действием эстрогенов, активно вырабатываемых в яичнике, пока там зреет очередная яйцеклетка.
Пролиферация в большей степени касается желез эндометрия, которые до овуляции должны максимально «удлинниться». В раннюю пролиферацию (5-7 день цикла) железы представлены узкими трубочками с темно окрашенными ядрами, но уже к 8-10 дню (средняя стадия фазы пролиферации) они начинают приобретать извитой вид, многочисленны митозы, что говорит об активном делении клеток. К 14 дню менструального цикла желез становится много, они извитые, ядра клеток находятся на разном уровне. К этому моменту пролиферация должна уступить место следующей фазе – секреции. Так происходит в норме.
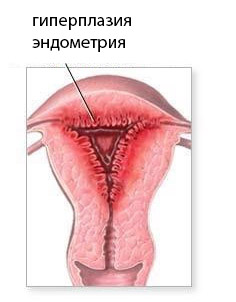 При патологии выраженная пролиферация компонентов эндометрия отражает гиперпластические процессы и опухоли.
Гиперплазия эндометрия – не что иное, как пролиферация, которая вовремя не остановилась, перейдя в секреторную фазу созревания слизистой оболочки. Усиленное размножение клеток эндометрия приводит к появлению избыточного железистого компонента, кистозной трансформации и чревато атипией.
При патологии выраженная пролиферация компонентов эндометрия отражает гиперпластические процессы и опухоли.
Гиперплазия эндометрия – не что иное, как пролиферация, которая вовремя не остановилась, перейдя в секреторную фазу созревания слизистой оболочки. Усиленное размножение клеток эндометрия приводит к появлению избыточного железистого компонента, кистозной трансформации и чревато атипией.
Выделают диффузную гиперплазию эндометрия, когда вся слизистая матки утолщена и не соответствует фазе цикла, и очаговую – полипы эндометрия. Полипы бывают пролиферативные, когда главным признаком становится деление железистого эпителия, и секреторные, больше характерные для второй фазы цикла.
Ключевым моментом в клинической оценке гиперплазии эндометрия становится наличие или отсутствие атипии (атипическая или неатипическая гиперплазия). Интенсивно делящиеся под действием гормонов клетки приобретают большую вероятность мутаций, поэтому атипия – вполне вероятное следствие пролиферации и гиперплазии.
При неатипической железистой гиперплазии пораженная ткань удаляется, а гинеколог решает вопрос о дополнительной консервативной терапии. Атипическая гиперплазия может потребовать более радикальных мер вплоть до удаления матки, хотя такие решения принимаются с учетом возраста, причин гиперплазии, репродуктивных планов женщины.
Таким образом, самостоятельного значения в качестве патологии пролиферация в матке не имеет, это не болезнь как таковая, она лишь отражает процессы, которые там происходят и может быть следствием как нормы, так и патологии. Отношение к пролиферации в матке определяется ее причинами и локализацией:
- В шейке без атипии на фоне воспаления, травм, эрозии – консервативное лечение;
- В шейке с атипией – удаление пораженного участка, консервативное лечение соответственно причине (гормоны, противомикробные препараты и т. д.);
- В эндометрии пролиферация в первую половину цикла – норма, нет поводов для беспокойства у пациентки репродуктивного возраста, в менопаузе любая пролиферация говорит о возобновлении роста эндометрия и требует пристального обследования (возможны гиперплазия, полип, рак);
- Пролиферация с гиперплазией – опасное явление, требующее выскабливания полости матки и гормонотерапии;
- Пролиферация с атипией – предраковое состояние, предполагающее удаление всего эндометрия или матки.
Опухолевая пролиферация означает увеличение объема ткани новообразования путем деления его клеток, часто – с атипией. Она не имеет самостоятельного значения, а лишь характеризует рост неоплазии, то есть, если есть опухоль, будет и пролиферация, а от ее выраженности зависит, как быстро вырастет неоплазия. Карциномы шейки матки, цервикального канала и всегда сопровождаются усиленной пролиферацией, которая заметна уже на стадии дисплазии.
Пролиферация в гастроэнтерологии
Пролиферация эпителия желудка происходит в норме и постоянно. Слизистая этого органа нуждается в регулярном обновлении, поэтому клетки активно делятся. В то же время, любое повреждение вызывает ускорение клеточного деления.
Основными причинами, вызывающими усиленную пролиферацию желудочного эпителия, считаются гастриты, язвы, полипы и опухоли. При остром гастрите на фоне выраженного воспалительного компонента в виде отека слизистой, слущивания поверхностного слоя, кровоизлияний обнаруживаются участки пролиферирующего покровно-ямочного эпителия, что отражает процесс регенерации слизистой оболочки.
Хронические гастриты , столь распространенные в наши дни во всех возрастных группах, тоже протекают с повышенной пролиферацией эпителия. Особенно явно этот процесс проявляется при гиперпластических формах заболевания, когда слизистая утолщается, возможны полиповидные разрастания.
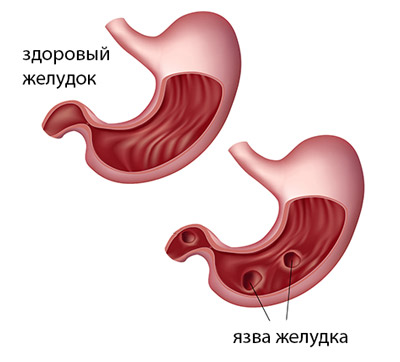 Язва желудка
при обострении протекает с повреждением стенки органа, которое организм стремится устранить. Результат – пролиферация эпителия, четко выраженная в краях язвенного дефекта. С такой пролиферацией связывают гиперпластические полипы, нередко обнаруживаемые в краях язвы.
Язва желудка
при обострении протекает с повреждением стенки органа, которое организм стремится устранить. Результат – пролиферация эпителия, четко выраженная в краях язвенного дефекта. С такой пролиферацией связывают гиперпластические полипы, нередко обнаруживаемые в краях язвы.
Особую опасность представляет предраковая пролиферация в стенке желудка , когда размножаться начинают темные вытянутые клетки из области шеек желудочных желез. Изначально этот процесс носит регенераторный характер, но так как дифференцировка клеток нарушена, то нормального восстановления слизистой не происходит. Вместо этого железы покрываются клетками с темными продолговатыми ядрами, располагающимися в их основании.
Предраковая пролиферация может иметь ограниченный или диффузный характер, но всегда обнаруживается в верхних отделах желез, при этом более глубокие слои остаются малоизмененными. Темные клетки диспластического эпителия не секретируют слизь и, соответственно, не выполняют свои прямые функции. Со временем, они вытесняют нормальную железистую выстилку, полностью ее замещая.
Следующим этапом такой пролиферации становится развитие , причем, это может быть небольшой участок одной железы. Злокачественная трансформация возникает в любой момент, но фоне имеющейся предраковой пролиферации и нормального строения других желез.
Молочная железа

Изменения молочной железы довольно распространены, в том числе, среди молодых девушек и женщин. Орган постоянно испытывает на себе действие половых гормонов, претерпевает характерные изменения на протяжении менструального цикла, при беременности и лактации, поэтому подвержен разного рода патологии. По статистике, до 60% женщин репродуктивного возраста имеют признаки мастопатии.
Мастопатию считают доброкачественным процессом, однако при ее наличии риск озлокачествления повышается в несколько раз. Пролиферативные варианты еще более опасны, они увеличивают вероятность рака в 25-30 раз.
Наличие или отсутствие пролиферации – важнейший признак при оценке разновидности мастопатии. Непролиферативные формы представлены очагами фиброзной ткани, кистозно измененными протоками, эпителий которых не пролиферирует и даже атрофичен. Риск злокачественной трансформации относительно мал.
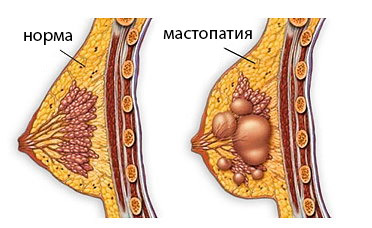 Пролиферативная мастопатия
куда опаснее, ведь клетки протоков и долек железы активно делятся, создавая угрозу ракового перерождения. Чем больше таких очагов пролиферации в ткани железы и чем активнее идет размножение эпителиального компонента, тем вероятнее в будущем, поэтому все формы пролиферирующей мастопатии считают предраковыми состояниями.
Пролиферативная мастопатия
куда опаснее, ведь клетки протоков и долек железы активно делятся, создавая угрозу ракового перерождения. Чем больше таких очагов пролиферации в ткани железы и чем активнее идет размножение эпителиального компонента, тем вероятнее в будущем, поэтому все формы пролиферирующей мастопатии считают предраковыми состояниями.
По выраженности пролиферации выделяют несколько степеней мастопатии. При первой степени пролиферация не обнаруживается, при второй – она есть, но клетки не имеют признаком атипии, третья степень мастопатии проявляется активной пролиферацией клеток эпителия с атипией.
Таким образом, пролиферация клеток молочной железы – не только критерий формы мастопатии, но и показатель вероятности рака, поэтому избыточное деление эпителия всегда привлекает внимание специалистов. Диагностику этого изменения проводят путем цитологического исследования полученной при пункции ткани.
Что делать при наличии пролиферации?
При обнаружении пролиферации где бы то ни было, специалист первым делом определит ее причину, а затем составит план ведения пациента. Не существует определенного способа лечения для пролиферации как таковой, ведь это не самостоятельная патология, а отражение других заболеваний. Если усиленное деление вызвано воспалением, то врач назначит противовоспалительную терапию, при необходимости дополнив ее антибактериальными или противовирусными средствами.
Предраковая пролиферация с атипией на фоне дисплазии может потребовать более радикальных мер – иссечения пораженного участка. В случае пролиферации на фоне лечение производится по всем принципам онкологической помощи вплоть до удаления органа.
Любая пролиферация, свидетельствующая о патологии, служит тревожным сигналом, поэтому пациенты с такими изменениями всегда находятся в поле зрения врача. После лечения основного заболевания обычно производится контрольное цитологическое исследование или биопсия, позволяющие оценить эффективность терапии и риск опухолевой трансформации в будущем.
Клеточные массы, составляющие узелок (обозначаемый термином «гра-нулема»), состоят из лимфоидных, эпителиоидных, плазматических клеток, не-редко с примесью гигантских с многочисленными ядрами. Цитологи-ческий состав гранулем варьирует в связи с разным количественным соот-ношением указанных элементов. Так, в центральных частях туберкулез-ных гранулем - бугорков отмечают скопления светлых эпителиоидных, а также гигантских клеток, а на периферии располагается зона лимфоидных клеток. Часто вокруг таких гранулем диффузно рассеяны плазматические клетки; последние могут вообще резко преобладать, образуя сплошные ин-фильтраты. Для гигантских клеток в туберкулезных бугорках типично пе-риферическое расположение ядер, образующих как бы кольцо или полуколь-цо (клетки Пирогова - Лангганса).
Гранулемы наблюдаются также при сифилисе, проказе, бруцеллезе, брюшном тифе, ревматизме, риносклероме, сапе, при вирусном энцефалите, риккетсиозах, например при сыпном тифе, при различных грибковых поражениях (актиномикоз, ас-пергиллез, бластомикоз и т.п.).
При сифилисе гранулемы (гуммы) состоят по преимуществу из лимфо-идных и плазматических клеток. Обычно речь идет о сливающихся инфильтратах, об-разующих крупные узлы величиной до куриного яйца и больше. Характерно обилие сосудов в периферических частях гумм и продуктивные процессы со стороны интимы сосудов, что часто приводит их к облитерации. Наряду с четко очерченными гуммами при сифилисе образуются диффузные гуммозные инфильтраты, например в мягких моз-говых оболочках.
При проказе гранулемы (лепромы) и диффузные инфильтраты отличаются обильным содержанием в них лепрозных бацилл. Бациллы располагаются в прото-плазме крупных «лепрозных клеток», называемых иногда «шарами» из-за округлых форм этих своеобразных макрофагов («клетки Вирхова»).
При бруцеллезе наряду с типичными милиарными * гранулемами, по сво-ему клеточному составу напоминающими туберкулезные бугорки, и даже чаще от-мечаются диффузные инфильтраты, например в мягких мозговых оболочках го-ловного и спинного мозга.
При брюшном тифе, при абдоминальной форме паратифа гранулемы, возни-кающие в лимфатическом аппарате кишечника (солитарные фолликулы, пейеровы бряшки), в печени, селезенке, иногда в гортани, желчных путях, имеют строение рас-плывчатых узелков из крупных ретикулярных клеток («тифозные клетки». При ревматизме гранулемы формируются, как правило, в плотных тканях, например, в фиброзных прослойках миокарда, в клапанах сердца, фасциях, апоневрозах, параартикулярных тканях. Это послужило основанием для отнесения острого ревматизма к «коллагенозам», т.е. к заболеваниям, в основе которых лежат те или иные формы дезорганизации коллагена, что и вызывает продуктивную кле-точную реакцию.
Ревматические гранулемы имеют то субмикроскопические размеры, то пред-ставляют собой узелки и узлы размером от рисового зерна до грецкого ореха. Они характеризуются пролиферацией крупных макрофагов (особенно в миокарде), а также лимфоцитов, фибробластов в виде розеток, палисадов. При риносклероме гранулемы представлены главным образом плазма-тическими и эпителиоидными клетками. Специфичны крупные «клетки Микулича», содержащие огромное количество палочек риносклеромы, а также своеобразные «гиа-линовые шары», являющиеся продуктом превращения цитоплазмы плазматических клеток. Процесс чаще всего локализуется в слизистой оболочке носа, глотки, гортани и ведет к сужению их просветов.
При сапе гранулематоз, вернее грануляционно-гнойные процессы, отмечается по преимуществу в дыхательных путях (нос, легкие), а также в коже. Гранулемы со-стоят из эпителиоидных клеток и лейкоцитов. Характерен распад клеток гранулем и диффузных инфильтратов с образованием обширных полей кариорексиса. Часты пере-ходы в вульгарное нагноение; гной отличается особой тягучестью.
Близкими являются изменения при сапоподобном заболевании, известном под на-званием мелиоидоз (болезнь тропических стран). При вирусных энцефалитах гранулемы развиваются по преимуществу в сером веществе центральной нервной системы; они состоят главным образом из кле-ток микроглии. Аналогичным образом выглядят гранулемы при сыпном тифе.
Гранулемы при грибковых заболеваниях бывают то ясно очерче-ны, то имеют вид диффузных инфильтратов, содержащих плазматические, эпителио-идные, гигантские клетки и соответствующие грибы в виде переплетающихся нитей или колоний звездчатой формы - Друз, видимых невооруженным глазом, например при а к т и н о микозе. Диагностически важно, что почти в 50% друзы отсутствуют, подвергаясь лизису, кальцинации, поглощению гигантскими клетками или пре-вращению в стекловидную массу (А. В. Талалаева и Д. И. Аснин, 1964). Характерно наличие на фоне обширных деревянистых склерозов рассеянных очажков нагноения, нередко свищевых ходов и образование в рубцовой ткани очагов ксантомных кле-ток.
Динамика гранулематозного процесса укладывается в следующие четыре фазы:
первичная альтерация ткани;
развитие клеточной гранулемы;
деструкция клеток гранулемы;
остаточный склероз, или инкапсуляция очага.
При первичной альтерации речь идет о дегенеративных и некробиотических из-менениях эндотелия сосуда, будущего центра гранулемы. Эти изменения стоят в связи с абсорбцией эндотелием тех или иных биологических и биохимических агентов, об-ладающих антигенными свойствами и способностью вызывать адекватную реакцию. Такими агентами могут быть циркулирующие в крови или лимфе микроорганизмы, их токсины, денатурированные собственные белки тела, инородные тела, случайно по-павшие в организм.
Первичная альтерация ткани часто сопряжена с тромбозом сосуда. Нередко свя-зи с сосудом обнаружить нельзя, и речь идет о первичной «дезорганизации» (В. Т. Та-лалаев, 1929) стромы, в частности коллагеновых волокон, как это происходит, напри-мер, при остром ревматизме. Центром будущей гранулемы могут стать подвергшиеся деструкции ганглиозные клетки, как это наблюдается при вирусных энцефалитах.
Вторая фаза развития гранулемы в морфологическом и гистогенетическом отно-шении скорее стереотипна, чем строго специфична в отношении, например, разных инфекций. И действительно, в состав гранулем входят по сути дела одни и те же клетки в различных соотношениях. Это понятно, так как клеточный материал, идущий на построение гранулем, имеет почти всегда один источник, а именно эндотелий, адвен-тициальные клетки, а также другие клетки мезенхимного происхождения. В построе-нии гранулем в нервной системе активное участие принимают клетки глии, а в полос-тях тела - клетки мезотелия. Цитологическое сходство гранулем при разных инфекционных заболеваниях на-ходит себе объяснение и в том, что сходными являются биологические основы грану-лематоза, а именно иммуногенез.
Цитологически гранулемы могут быть построены с некоторым своеобразием. Так, в одних много гигантских клеток, в других их совсем нет, в одних резко пре-обладают эпителиоидные клетки, а в других - лимфоидные, плазматические и т.д. Это позволяет практически ориентироваться в распознавании природы болезни.
Однако указанное своеобразие связано не только с особенностями агента, на-пример инфекта, но и с особенностями организма, не говоря о специфичности суб-страта, т.е. месте развития гранулемы. Другими словами, три величины определяют гранулематоз и его конкретное морфологическое выражение, причем каждая из этих величин (агент, организм, ткань или орган) обладает всегда каким-то диапазоном лабильности.
Непосредственным стимулом гранулематоза являются химические вещества, воз-никающие в процессе первичной альтерации. Это могут быть продукты тканевой дена-турации, в частности вещества, обладающие свойствами аутоадлергенов, продукты жизнедеятельности микроорганизмов, а также продукты их распада. Типичные ту-беркулезные гранулемы можно получить, вводя мертвые туберкулезные бациллы (Koch, 1884; В. К. Высокович, 1890) и даже химические вещества, получаемые в про-цессе их обработки (воски, фосфатиды и др.). Эти химические вещества часто оказыва-ются общими у различных микробов. Вот почему типичные для туберкулеза бугорки с гигантскими клетками и творожистым некрозом можно получить, вводя фосфатиды, извлеченные из бацилл тимофеевой травы, из лепрозных палочек.
Третья фаза - деструкция клеток гранулемы - выражается или в некрозе центра гранулемы (творожистый некроз при туберкулезе, гуммозный распад при си-филисе), или в постепенно прогрессирующей дегенерации ее клеток, незаметной на фоне превращения гранулемы в очаг склероза. Деструкция может получить черты колликвационного некроза, т.е. разжижения, а иногда черты нагноения (сап, тубер-кулез, грибковые поражения). В последнем случае завершающий склероз бывает осо-бенно обширным.
Клиническое значение гранулематоза часто определяется именно склерозами (четвертая фаза), их месторасположением и общей площадью. Ревматические склерозы, возникающие по ходу проводящей системы сердца, влекут за собой нарушения проводимости возбуждения на пути от синусового узла к камерам сердца вплоть до так называемой блокады сердца. Гранулематоз при сифилитическом поражении аорты, сопровождаясь распадом эластических структур, лежит в основе аневризматических расширений аорты. Различные деформации органов в виде дольчатой печени, легкого (hepar lobatum, pulmo lobatum), саблевидных ног, западения спинки носа, облитерации просветов сосудов и пр. характеризуют сифилитический гранулематоз соответствующей локализации.
Нарушения белкового обмена в виде амилоидоза часто оказываются следствием рецидивирующих форм гранулематоза при туберкулезе, актиномикозе, особенно при сочетании этих инфекций с обширным распадом и нагноением. Полное выпадение функции надпочечников при аддисоновой болезни обычно имеет своей основой диф-фузный туберкулезный гранулематоз их. Сравнительно острым по своему течению является вирусный и риккетсиозный гранулематоз центральной нервной системы, который может не оставлять после себя никаких не только клинических, но даже и анатомических последствий (например, сыпной тиф). Чаще, однако, весь цикл развития гранулем охватывает значительные сроки, на-пример месяц и более, и остаточные явления, т.е. склерозы, бывают заметными. Это сближает пролиферативное воспаление с хроническими его формами, где каждый цикл завершается образованием рубца.
Другое свойство пролиферативных форм воспаления заключается в их тен-денции рецидивировать после заживления спустя месяцы, иногда годы и десятки лет (бруцеллез, туберкулез, ревматизм, сифилис и др.).
Вопрос о причинах того, почему воспалительные процессы принимают черты гра-нулематоза, что сочетается с удлинением сроков течения заболевания, принимающего часто характер хронического, современной патологией решается с иммунологических позиций.
Другими словами, гранулематоз не является каким-то односторонним или спе-цифическим свойством инфекта, т.е. микроба-возбудителя. Гранулематоз следует рас-сматривать как морфологическое выражение своеобразных иммунологических отно-шений между «хозяином» и «гостем», т.е. между организмом и инфектом. Гранулема-тоз, следовательно, отражает динамику иммунизаторного процесса, его этапы и количе-ственные вариации.
Насколько велики бывают количественные вариации, свидетельствуют случаи милиарного туберкулеза (т.е. образования неисчислимого количества мельчайших гранулем), с одной стороны, и случаи единичных, случайно обнаруживаемых грану-лем - с другой.
Лейшмании (Leishmania tropica), класса простейших. Являются возбуди-телями кожного лейшманиоза, называемого пендинской, или восточной, яз-вой, а также висцеральных поражений (калаазар). Кожный процесс возникает на месте укуса насекомого (флеботомус) сначала в виде узелка, который затем изъязвля-ется. Типично образование множественных гранулем из эпителиоидных клеток, со-держащих лейшмании.
Ф и л я р и и (Filaria Bancrofti), класса нематод. Являются возбудителями фи-ляриоза; передаются москитами. Процесс локализуется в коже по ходу лимфати-ческой системы и носит хронический характер; сопровождается гиперпродукцией со-единительной ткани, так называемой слоновостью (elephantiasis) нижних конечностей, мошонки с распространением на забрюшинную клетчатку, хроническим лимфангитом и лимфаденитом.
Финна эхинококкового солитера (Taenia echinococcus), парази-тирующего в кишечнике собак, обозначается эхинококком, который может быть одно-камерным и многокамерным, а величиной от кедрового ореха до головы взрослого че-ловека. Продуктивные процессы особенно обширны при многокамерном эхинококке печени.
Такой же как бы ареактивный симбиоз наблюдается в центральной нервной сис-теме при некоторых спирохетозах, например при прогрессивном параличе, возвратном тифе.
В развитии низших и высших позвоночных отчетливо прослеживается единая общебиологическая закономерность, выражающаяся в появлении зародышевых листков и обособлении основных зачатков органов и тканей. Процесс образования тканей из материала эмбриональных зачатков составляет суть учения о гистогенезах.
Эмбриональный гистогенез , по определению А.А. Клишова (1984), - это комплекс координированных во времени и пространстве процессов пролиферации, клеточного роста, миграции, межклеточных взаимодействий, дифференциации, детерминации, программированной гибели клеток и некоторых других. Все названные процессы в той или иной мере протекают в зародыше, начиная с самых ранних стадий его развития.
Пролиферация . Основной способ деления тканевых клеток - это митоз. По мере увеличения числа клеток возникают клеточные группы, или популяции, объединенные общностью локализации в составе зародышевых листков (эмбриональных зачатков) и обладающие сходными гистогенетическими потенциями. Клеточный цикл регулируется многочисленными вне- и внутриклеточными механизмами. К внеклеточным относятся влияния на клетку цитокинов, факторов роста, гормональных и нейрогенных стимулов. Роль внутриклеточных регуляторов играют специфические белки цитоплазмы. В течение каждого клеточного цикла существуют несколько критических точек, соответствующих переходу клетки из одного периода цикла в другой. При нарушении внутренней системы контроля клетка под влиянием собственных факторов регуляции элиминируется апоптозом, либо на некоторое время задерживается в одном из периодов цикла.
Метод радиографического анализа клеточных циклов в различных тканях выявил особенности соотношения клеточной репродукции и дифференцировки. Например, если в тканях (кроветворные ткани, эпидермис) имеется постоянный фонд пролиферирующих клеток, за счет которых обеспечивается непрерывное возникновение новых клеток взамен погибающих, то эти ткани относятся к обновляющимся. Другие ткани, например, некоторые соединительные, характеризуются тем, что в них увеличение количества клеток происходит параллельно с их дифференцировкой, клетки в этих тканях характеризуются низкой митотической активностью. Это растущие ткани. Наконец, нервная ткань характеризуется тем, что все основные процессы репродукции заканчиваются в период эмбрионального гистогенеза (когда формируется основной запас стволовых клеток, достаточный для последующего развития ткани). Поэтому она отнесена к стабильным (стационарным) тканям. Продолжительность жизни клеток в обновляющихся, растущих и стабильных тканях разная.
Наряду с обновлением клеточной популяции , в самих клетках постоянно наблюдается обновление внутриклеточных структур (внутриклеточная физиологическая регенерация).
Клеточный рост, миграция и межклеточные взаимодействия . Рост клеток проявляется в изменении их размеров и формы. При усилении функциональной активности и внутриклеточных биосинтезов наблюдается увеличение объема клетки. Если объем клетки превышает некую норму, то говорят о ее гипертрофии, и наоборот, при снижении функциональной активности происходит уменьшение объема клетки, а при переходе некоторых нормативных параметров возникает атрофия клетки. Рост клетки не беспределен и определяется оптимальным ядерно-цитоплазменным отношением.
Важное значение для гистогенеза имеют процессы перемещения клеток . Миграция клеток наиболее характерна для периода гаструляции. Однако и в период гисто- и органогенеза происходят перемещения клеточных масс (например, смещения миобластов из миотомов в места закладки скелетных мышц; движение клеток из нервного гребня с образованием спинномозговых ганглиев и нервных сплетений, миграция гоноцитов и т. д.). Миграция осуществляется с помощью нескольких механизмов. Так, различают хемотаксис - движение клеток в направлении градиента концентрации какого-либо химического агента (перемещения спермиев к яйцеклетке, предшественников Т-лимфоцитов из костного мозга в закладку тимуса).
Гаптотаксис - механизм перемещения клеток по градиенту концентрации адгезионной молекулы (движение клеток протока пронефроса у амфибий по градиенту щелочной фосфатазы на поверхности мезодермы). Контактное ориентирование - когда в какой-либо преграде остается один канал для перемещения (описан у рыб при образовании плавников).
Контактное ингибирование - этот способ перемещения наблюдается у клеток нервного гребня. Суть способа заключается в том, что при образовании ламеллоподии одной клеткой и контакта ее с другой клеткой, ламеллоподия прекращает рост и постепенно исчезает, но в другой части мигрирующей клетки при этом формируется новая ламеллоподия.
В процессе миграции клеток важную роль играют межклеточные взаимодействия. Существует несколько механизмов такого взаимодействия (контактного и дистантного). Выделяется большая группа молекул клеточной адгезии (МКА). Так, кадгерины - это Са2+-зависимые МКА, отвечают за межклеточные контакты при образовании тканей, за формообразование и др. В молекуле кадгерина различают внеклеточный, трансмембранный и внутриклеточный домены. Например, внеклеточный домен ответственен за адгезию клеток с одинаковыми кадгеринами, а внутриклеточный - за форму клетки. Другой класс МКА - это иммуноглобулиновое суперсемейство Са2+-независимых МКА, обеспечивающих, например, адгезию аксонов к сарколемме мышечных волокон, или миграцию нейробластов вдоль радиальных глиоцитов в закладке коры большого мозга и др. Следующий класс МКА - это мембранные ферменты - гликозилтранферазы. Последние по типу "ключ-замок" соединяются с углеводными субстратами - гликозаминогликанами надмембранного комплекса клетки, осуществляя таким образом прочное сцепление клеток.
Кроме механизмов межклеточного взаимодействия , существуют механизмы взаимодействия клеток с субстратом. Они включают формирование рецепторов клетки к молекулам внеклеточного матрикса. К последним относят производные клеток, среди которых наиболее изученными адгезионными молекулами являются коллаген, фибронектин, ламинин, тенасцин и некоторые другие. Коллагены, среди которых различают несколько десятков типов, входят в состав межклеточного вещества рыхлой волокнистой соединительной ткани, базальной мембраны и пр. Фибронектин, секретируемый клетками, является связывающей молекулой между мигрирующей клеткой и межклеточным матриксом. Ламинин - компонент базальной мембраны, также связывает мигрирующие клетки с межклеточным матриксом (справедливо по отношению к эпителиоцитам и нейробластам).
Для осуществления связи мигрирующих клеток с межклеточным матриксом клетки формируют специфические рецепторы. К ним относятся, например, синдекан, который обеспечивает контакт эпителиоцита с базальной мембраной за счет сцепления с молекулами фибронектина и коллагена. Интегрины клеточных поверхностей связывают с внеклеточной стороны молекулы внеклеточного матрикса, а внутри клетки - белки цитоскелета (например, актиновые микрофиламенты). Так возникает связь внутри- и внеклеточных структур, что позволяет клетке использовать для перемещения собственный сократительный аппарат. Наконец, существует большая группа молекул, формирующих клеточные контакты, осуществляющие коммуникацию между клетками (щелевые контакты), механическую связь (десмосомы, плотные контакты).
Дистантные межклеточные взаимодействия осуществляются путем секреции гормонов и факторов роста (ФР). Последние - это вещества, оказывающие стимулирующее влияние на пролиферацию и дифференцировку клеток и тканей. К ним относятся, например, ФР, полученный из тромбоцитов и влияющий на переход клеток в фазу размножения (гладких миоцитов, фибробластов, глиоцитов); эпидермальный ФР - стимулирует пролиферацию эпителиоцитов, производных эктодермы; ФР фибробластов - стимулирует пролиферацию фибробластов. Особо выделяется большая группа пептидов (соматотропины, соматомедины, инсулин, лактоген), влияющих на развитие клеток плода.














